摘要: 共价键的分类:极性键.非极性键 项目 共价键 极性键 非极性键 共用电子对偏移程度 构成元素 实例
网址:http://m.1010jiajiao.com/timu_id_3649048[举报]
组成蛋白质的元素主要有C、H、O、N及S、P和少量的Cu、Fe、Zn等,其中铜及其合金是人类最早使用的金属材料,用途广泛.
(1)铜原子的核外电子排布式是________;O、N、S的第一电离能由大到小的顺序为________.
(2)铜的熔点比钙高,其原因是________;下图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为________.

(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物.
①[Cu(NH3)4]2+中存在的化学键类型有________(填序号).
A.配位键
B.金属键
C.极性共价键
D.非极性共价键
E.离子键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为________(填序号).
A.平面正方形
B.正四面体
C.三角锥型
D.V型
③某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:
HOCH2CH=CH2→CH3CH2CHO.在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为________.
 (1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:| 电离能(kJ?mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
能量最低原理
能量最低原理
、泡利原理
泡利原理
,B元素位于周期表五个区域中的S
S
区.②ACl2分子中A的杂化类型为
SP
SP
,ACl2空间构型为直线
直线
.(2)Fe原子或离子外围有较多能量相近的空轨道,所以其能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
具有孤对电子
具有孤对电子
.②六氰合亚铁离子[Fe(CN)6]4-中不存在
B
B
.A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
写出一种与CN-互为等电子体的单质的分子式
N2
N2
.(3)一种Al-Fe合金的立体晶胞如图2所示,请据此回答下列问题:
①确定该合金的化学式
Fe2Al
Fe2Al
.②若晶体的密度为ρg?cm-3,该晶胞棱长为
| 3 |
| ||
| 3 |
| ||
下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是 (填编号)
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是 (写分子式).元素⑨和⑩形成的化合物的化学式为 ,它是一种重要的结构材料,推测它应是属于 晶体;元素①的原子价电子排布式是 .
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是 键(填σ或π),在高中化学中有一种常见分子的结合方式与O3相同,它是 (填分子式).
(4)③和⑨两元素比较,非金属性较弱的是 (填名称),可以验证你的结论的是下列中的 (填序号).
A、气态氢化物的挥发性和稳定性
B、单质分子中的键能
C、两元素的电负性
D、最高价含氧酸的酸性
E、氢化物中X-H键的键长(X代表③和⑨两元素)
F、两单质在自然界的存在形式.
查看习题详情和答案>>
| 元素 性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
| 原子半径 (10-10m) |
1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是
(4)③和⑨两元素比较,非金属性较弱的是
A、气态氢化物的挥发性和稳定性
B、单质分子中的键能
C、两元素的电负性
D、最高价含氧酸的酸性
E、氢化物中X-H键的键长(X代表③和⑨两元素)
F、两单质在自然界的存在形式.
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
①某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了______、______,B元素位于周期表五个区域中的______区.
②ACl2分子中A的杂化类型为______,ACl2空间构型为______.
(2)Fe原子或离子外围有较多能量相近的空轨道,所以其能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氰合亚铁离子[Fe(CN)6]4-中不存在______.
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
写出一种与CN-互为等电子体的单质的分子式______.
(3)一种Al-Fe合金的立体晶胞如图2所示,请据此回答下列问题:
①确定该合金的化学式______.
②若晶体的密度为ρg-cm-3,该晶胞棱长为______cm(用含ρ和NA的代数式表示,不必化简.
查看习题详情和答案>>
| 电离能(kJ-mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
②ACl2分子中A的杂化类型为______,ACl2空间构型为______.
(2)Fe原子或离子外围有较多能量相近的空轨道,所以其能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氰合亚铁离子[Fe(CN)6]4-中不存在______.
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
写出一种与CN-互为等电子体的单质的分子式______.
(3)一种Al-Fe合金的立体晶胞如图2所示,请据此回答下列问题:
①确定该合金的化学式______.
②若晶体的密度为ρg-cm-3,该晶胞棱长为______cm(用含ρ和NA的代数式表示,不必化简.

下表列出前20号元素中的某些元素性质的一些数据:
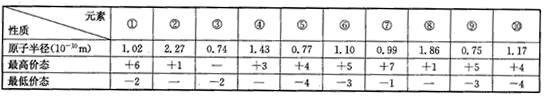
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是__(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是____(写分子式)。元素⑨和⑩形成的化合物的化学式为_________,它是一种 ____晶体,是重要的结构材料;元素①的原子价电子排布式是____。
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°。三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键——三个原子均等地享有这四个电子,这种特殊的共价键的类型是____键(填“σ”或“π”),在高中化学中有一种常见分子的结合方式与O3相同,它是____(填分子式)。
(4)⑥和⑨两元素比较,非金属性较弱的是____(填名称),可以验证你的结论的是下列中的__________(填序号)。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表⑥和⑨两元素)
F.两单质在自然界的存在形式
查看习题详情和答案>>
(1)以上10种元素中,第一电离能最小的是__(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是____(写分子式)。元素⑨和⑩形成的化合物的化学式为_________,它是一种 ____晶体,是重要的结构材料;元素①的原子价电子排布式是____。
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°。三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键——三个原子均等地享有这四个电子,这种特殊的共价键的类型是____键(填“σ”或“π”),在高中化学中有一种常见分子的结合方式与O3相同,它是____(填分子式)。
(4)⑥和⑨两元素比较,非金属性较弱的是____(填名称),可以验证你的结论的是下列中的__________(填序号)。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表⑥和⑨两元素)
F.两单质在自然界的存在形式