网址:http://m.1010jiajiao.com/timu_id_3647100[举报]
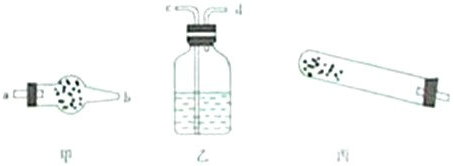
(1)若用如图所示仪器对分解产物中的非固体氧化物进行验证.则碱式碳酸铜应该放在
(2)将碱式碳酸铜与过量的木炭混合加热,可能得到铜、一氧化碳和水三种物质,该反应的化学方程式是
| ||
| ||
(3)铜及其合金用途广泛,常见的铜的合金有黄铜(铜锌合金)、青铜(铜锡合金).现有w g黄铜样品,放入足量的橘盐酸中,产生V mL气体(标准状况下),则样品中铜和锌的物质的量之比是
| 22400w-65V |
| 64V |
| 22400w-65V |
| 64V |
碱式碳酸铜是孔雀石的主要成分,加热时可分解为氧化铜、二氧化碳和水三种氧化物.
(1)若用下列仪器对分解产物中的非固体氧化物进行验证,仪器接口顺序是______(填字母).

按仪器连接顺序将仪器名称和对应仪器所装药品的名称填入下表.
| 仪器 | 试管 | ______ | ______ |
| 药品 | 碱式碳酸铜 | ______ | ______ |
(2)待(1)加热分解完全的试管冷却后,加入盐酸充分反应,CuO部分溶解,过滤:
①所得滤液中各种离子的物质的量浓度由大到小的顺序是______.
②将滤渣洗涤干燥,置于酒精蒸汽中并加热,黑色粉状固体逐渐变成红色固体,同时产生一种在常温下有刺激性气味的液体,该反应的化学方程式是______.
(3)将碱式碳酸铜与过量的木炭混合加热,也能得到(2)②所得的红色固体,该反应的化学方程式是______.
(4)铜及其合金用途广泛,常见的铜的合金有黄铜(铜锌合金)、青铜(铜锡合金)等.现有 w g黄铜样品,放入足量的稀盐酸中,产生V mL气体(标准状况下),则样品中铜和锌的物质的量之比是______(用含w、V的代数式表示). 查看习题详情和答案>>
(1)若用下列仪器对分解产物中的非固体氧化物进行验证,仪器接口顺序是______(填字母).

按仪器连接顺序将仪器名称和对应仪器所装药品的名称填入下表.
| 仪器 | 试管 | ______ | ______ |
| 药品 | 碱式碳酸铜 | ______ | ______ |
(2)待(1)加热分解完全的试管冷却后,加入盐酸充分反应,CuO部分溶解,过滤:
①所得滤液中各种离子的物质的量浓度由大到小的顺序是______.
②将滤渣洗涤干燥,置于酒精蒸汽中并加热,黑色粉状固体逐渐变成红色固体,同时产生一种在常温下有刺激性气味的液体,该反应的化学方程式是______.
(3)将碱式碳酸铜与过量的木炭混合加热,也能得到(2)②所得的红色固体,该反应的化学方程式是______.
(4)铜及其合金用途广泛,常见的铜的合金有黄铜(铜锌合金)、青铜(铜锡合金)等.现有 w g黄铜样品,放入足量的稀盐酸中,产生V mL气体(标准状况下),则样品中铜和锌的物质的量之比是______(用含w、V的代数式表示).
(1)若用下列仪器对分解产物中的非固体氧化物进行验证,仪器接口顺序是 (填字母).

按仪器连接顺序将仪器名称和对应仪器所装药品的名称填入下表.
| 仪器 | 试管 | ||
| 药品 | 碱式碳酸铜 |
(2)待(1)加热分解完全的试管冷却后,加入盐酸充分反应,CuO部分溶解,过滤:
①所得滤液中各种离子的物质的量浓度由大到小的顺序是 .
②将滤渣洗涤干燥,置于酒精蒸汽中并加热,黑色粉状固体逐渐变成红色固体,同时产生一种在常温下有刺激性气味的液体,该反应的化学方程式是 .
(3)将碱式碳酸铜与过量的木炭混合加热,也能得到(2)②所得的红色固体,该反应的化学方程式是 .
(4)铜及其合金用途广泛,常见的铜的合金有黄铜(铜锌合金)、青铜(铜锡合金)等.现有 w g黄铜样品,放入足量的稀盐酸中,产生V mL气体(标准状况下),则样品中铜和锌的物质的量之比是 (用含w、V的代数式表示). 查看习题详情和答案>>
三草酸合铁(Ⅲ)酸钾晶体(K3[Fe(C2O4)3]·3H2O)有很重要的用途。可用如下流程来制备。根据题意完成下列各题:

(1)要从溶液中得到绿矾,必须进行的实验操作是 。(按前后顺序填)
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4— 被还原成Mn2+。向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性。
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00ml,滴定中MnO4—,被还原成Mn2+。
(2)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有 ;
主要操作步骤依次是:称量、溶解、转移、 、定容、摇匀。
(3)步骤2中,加入锌粉的目的是 。
(4)步骤3中,发生反应的离子方程式为: 。
(5)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量 。(选填“偏低”、“偏高”、“不变”)
(6)某同学将8.74 g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647 g/L(已折合成标准状况下)气体(是物质的量之比为4:5的混合气体)。研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3。写出该分解反应的化学方程式 。
查看习题详情和答案>>