摘要:某学生称量CuSO4·5H2O时.左盘放砝码4 g.游码在0.5刻度处.天平平衡.右盘CuSO4·5H2O晶体的质量是 ( ) A.4.5 g B.4 g C.3.5 g D.3 g
网址:http://m.1010jiajiao.com/timu_id_3642960[举报]
已知在pH为4-5的环境中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生欲用电解纯净的CuSO4溶液的方法,根据电极上析出铜的质量以及电极上产生气体的体积来测定铜的相对原子质量.其实验过程如下图所示:
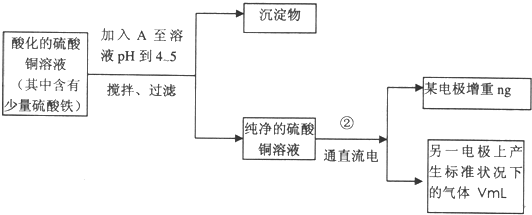
(1)符合条件的A可能是
a.NH3?H2O b.Cu c.CuO d.Cu(OH)2
(2)过滤操作中用到的玻璃仪器有
(3)电解开始一段时间后,在U形管中观察到的现象有
(4)下列实验操作中必要的是(填字母)
A.称量电解前电极的质量
B.电解后,电极在烘干称重前,必须用蒸馏水冲洗
C.刮下电解后电极上析出的铜,并清洗、称重
D.电极在烘干称重的操作中必须按“烘干-称重-再烘干-再称重”进行
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为
(用带有n、V的计算式表示).
查看习题详情和答案>>

(1)符合条件的A可能是
cd
cd
a.NH3?H2O b.Cu c.CuO d.Cu(OH)2

(2)过滤操作中用到的玻璃仪器有
烧杯、玻璃棒、漏斗
烧杯、玻璃棒、漏斗
;步骤②中所用的部分仪器如图,则A连接直流电源的负
负
极,B电极上发生的电极反应为40H--4e-═02↑+2H20
40H--4e-═02↑+2H20
.(3)电解开始一段时间后,在U形管中观察到的现象有
铜棒变粗,石墨极上有气泡生成,溶液的颜色变浅
铜棒变粗,石墨极上有气泡生成,溶液的颜色变浅
电解的离子方程式为2Cu2++2H20
2Cu+4H++02↑
| ||
2Cu2++2H20
2Cu+4H++02↑
.
| ||
(4)下列实验操作中必要的是(填字母)
ABDE
ABDE
.A.称量电解前电极的质量
B.电解后,电极在烘干称重前,必须用蒸馏水冲洗
C.刮下电解后电极上析出的铜,并清洗、称重
D.电极在烘干称重的操作中必须按“烘干-称重-再烘干-再称重”进行
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为
| 11200n |
| V |
| 11200n |
| V |
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.其实验流程图如下:
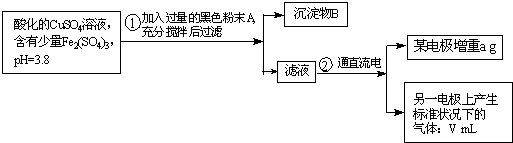
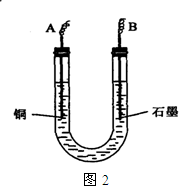
试回答下列问题:
(1)步骤①中加入A的化学式为 ,其作用是 ;沉淀物B是 (填化学式).
(2)步骤②中所用部分仪器如右2图所示:则A应连接直流电源的 极.
(3)下列实验操作属不必要的是 (填字母).
A.称量电解前电极的质量
B.电解后电极在烘干前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称量
D.电极在烘干称重的操作中必须按如下顺序:烘干→称重→再烘干→再称重进行两次
E.在空气中烘干电极,必须采用低温烘干法
(4)电解后向溶液中加入石蕊试液,观察到的现象是 .
查看习题详情和答案>>


试回答下列问题:
(1)步骤①中加入A的化学式为
(2)步骤②中所用部分仪器如右2图所示:则A应连接直流电源的
(3)下列实验操作属不必要的是
A.称量电解前电极的质量
B.电解后电极在烘干前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称量
D.电极在烘干称重的操作中必须按如下顺序:烘干→称重→再烘干→再称重进行两次
E.在空气中烘干电极,必须采用低温烘干法
(4)电解后向溶液中加入石蕊试液,观察到的现象是
已知pH为4-5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(n)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,过程如图1:
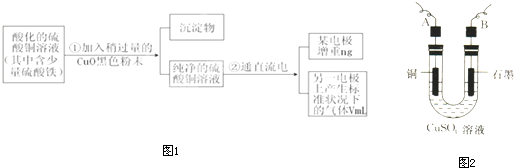
回答下列问题:
(1)加入CuO的作用是
(2)步骤②中所用的部分仪器如图2所示,则A、B分别连直流电源的
(3)电解开始后,在U形管中可以观察到的现象有:
(4)下列实验操作中必要的是
a.电解前的电极的质量;b.电解后,电极在烘干称量前,必须用蒸馏水冲洗;c.刮下电解后电极上析出的铜,并清洗,称量;d.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;e.在有空气存在的情况下,烘干电极必须用低温烘干的方法.
(5)铜的相对原子质量为
(用带有n、V的计算式表示).
查看习题详情和答案>>

回答下列问题:
(1)加入CuO的作用是
消耗H+而调整溶液的pH使之升高,使Fe3+完全水解形成Fe(OH)3沉淀而除去
消耗H+而调整溶液的pH使之升高,使Fe3+完全水解形成Fe(OH)3沉淀而除去
.(2)步骤②中所用的部分仪器如图2所示,则A、B分别连直流电源的
负
负
和正
正
极(填“正”或“负”).(3)电解开始后,在U形管中可以观察到的现象有:
铜棒变粗,石墨极上有气泡生成,溶液的颜色变浅
铜棒变粗,石墨极上有气泡生成,溶液的颜色变浅
.电解的离子方程式为2Cu2++2H2O
2Cu↓+O2↑+4H+;
| ||
2Cu2++2H2O
2Cu↓+O2↑+4H+;
.
| ||
(4)下列实验操作中必要的是
abde
abde
(填写字母).a.电解前的电极的质量;b.电解后,电极在烘干称量前,必须用蒸馏水冲洗;c.刮下电解后电极上析出的铜,并清洗,称量;d.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;e.在有空气存在的情况下,烘干电极必须用低温烘干的方法.
(5)铜的相对原子质量为
| 11200 |
| V |
| 11200 |
| V |
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.其实验流程如图1所示:
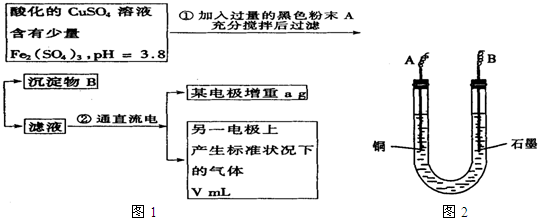
试回答下列问题:
(1)步骤①所加入的A的化学式为 ;加入A的作用是 ;沉淀物B是 (填化学式).
(2)步骤②中所用部分仪器如图2所示:则A应接直流电源的 极,B电极上发生的电极反应式为 .
(3)下列实验操作属必要的是 (填字母).
A.称量电解前电极的质量
B.电解后电极在烘干前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称量
D.电极在烘干称重的操作中必须按:烘干→称重→再烘干→再称重进行两次
E.在空气中烘干电极时,必须采用低温烘干法
(4)电解后向溶液中加入石蕊试液,观察到的现象是 .
(5)铜的相对原子质量的计算式为 .
查看习题详情和答案>>

试回答下列问题:
(1)步骤①所加入的A的化学式为
(2)步骤②中所用部分仪器如图2所示:则A应接直流电源的
(3)下列实验操作属必要的是
A.称量电解前电极的质量
B.电解后电极在烘干前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称量
D.电极在烘干称重的操作中必须按:烘干→称重→再烘干→再称重进行两次
E.在空气中烘干电极时,必须采用低温烘干法
(4)电解后向溶液中加入石蕊试液,观察到的现象是
(5)铜的相对原子质量的计算式为
(2009?大连一模)细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”.其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O═2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式:
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
实验室有下列试剂可供选择A. H2O2 B.CaO C.CuO D.稀H2SO4 E.铁粉;
实验经过滤后还需设计的实验操作步骤和目的是:
(3)若向CuSO4、FeSO4混合液中加入适量碱液,将溶液蒸干、灼烧得到红色粉末是Fe2O3、Cu2O混合物,欲测定该混合物中Cu2O的质量分数.该实验小组的方法是向m g混合物中加入足量的稀硫酸,经过滤、洗涤、干燥、称量固体的质量为n g.已知Cu2O溶于稀硫酸生成Cu和CuSO4.某学生据此计算出该混合物Cu2O的质量分数的计算式
×100%.该学生的计算是否正确:
查看习题详情和答案>>
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式:
4FeSO4+2H2SO4+O2
2Fe2(SO4)3+2H2O
| ||
4FeSO4+2H2SO4+O2
2Fe2(SO4)3+2H2O
.
| ||
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | 加入H2O2 加入H2O2 |
把二价铁氧化成三价 把二价铁氧化成三价 |
| 步骤2 | 加入适量氧化铜,调节pH到3.7 加入适量氧化铜,调节pH到3.7 |
保证三价铁完全沉淀 保证三价铁完全沉淀 |
| 步骤3 | 过滤 过滤 |
滤出氢氧化铁 滤出氢氧化铁 |
| 步骤4 | 洗涤 | 除去杂质 除去杂质 |
| 步骤5 | 向沉淀中加入适量稀硫酸和适量铁粉 向沉淀中加入适量稀硫酸和适量铁粉 |
得到FeSO4溶液 |
| 144n |
| 64m |
不正确
不正确
,请说明理由因为该计算没有考虑Cu与Fe3+的反应
因为该计算没有考虑Cu与Fe3+的反应
.