摘要:27.某温度下.向100ml 2mol/L的盐酸中加入铁粉2.8克.反应进行到2秒时放出氢气0.56L.反应又进行了4秒后铁粉全部溶解.(假设反应过程中溶液体积保持不变)试计算:(1)前2秒内用HCl表示的平均反应速率为 ?(2)后4秒内用FeCl2表示的平均反应速率为 ?(3)前2秒和后4秒相比.化学反应速率哪个快?为什么? 高 一 期 中 化 学 答 题 卷姓名 班级 学号 成绩 21.(1) 周期 族.(2) (3) ______ ______________________
网址:http://m.1010jiajiao.com/timu_id_349348[举报]
一、选择题。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
D
B
D
B
C
A
C
A
A
D
A
C
D
D
D
C
C
C
C
A
二、填空题。
 21.(每空1分,共10分)(1)Na,Ar 钠、钙、锡、硒 第四周期ⅣB族
21.(每空1分,共10分)(1)Na,Ar 钠、钙、锡、硒 第四周期ⅣB族
(2) H C H Na+[ Cl ]-
(3)非金属 -3 H3PO4 3NaOH+H3PO4=Na3PO4+3H2O
22.(每空2分,共14分)
(1)A氢,B钠,C硫,D铝,E钾
(2)Al(OH)3+
 |
(3)K + S + K → K+[ S ]2-K+
23.(每空2分,共4分)属于放热反应的是①②④⑦⑧ 属于吸热反应的是③⑤⑥
三、实验题
24.(12分)(1)探究同主族元素性质相似性和递变性
(2)试管、烧杯、胶头滴管
(3)
实验方案
实验现象
离子方程式
①
D
Cl2+2Br-=2Cl-+Br2
②
A
2Na+2H2O=2Na++2OH-+H2↑
③
B
Br2+2I-=2Br-+I2
④
C
2K+2H2O=2K+2OH-+H2↑
 25.(1)(4分)负极反应式:Fe-2e-=Fe2+
25.(1)(4分)负极反应式:Fe-2e-=Fe2+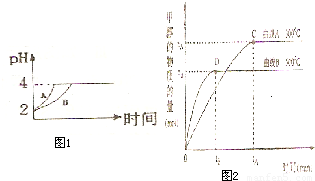
 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题: NH3?H2O+H+
NH3?H2O+H+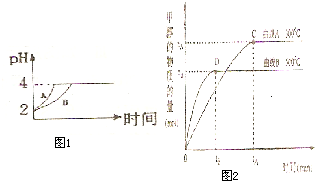 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: