摘要:现 象反应前质量(g)反应后质量(g)B装置中逐渐变成亮红色
网址:http://m.1010jiajiao.com/timu_id_344413[举报]
 (1)化学是一门以实验为基础的学科,取用块状药品通常用
(1)化学是一门以实验为基础的学科,取用块状药品通常用镊子
镊子
,取用一定量的液体时需要胶头滴管和量筒
胶头滴管和量筒
,实验结束时要洗涤仪器,玻璃仪器洗涤干净的标志是当洗过的玻璃仪器内壁的水既不聚成水滴也不成股流下时,表示已洗干净
当洗过的玻璃仪器内壁的水既不聚成水滴也不成股流下时,表示已洗干净
.(2)在“氧气的制取和性质”实验中,某同学取一段纱窗网上还能任意弯曲的细铁丝,在新制的氧气中做“铁丝燃烧”的实验.结果没有观察到“火星四射”的现象,请分析此实验失败的原因
铁丝表面有锈
铁丝表面有锈
(写一种);经过改进后实验成功了,其反应的符号表达式3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
.实验时要在集气瓶底部铺一层细沙或装少量水的原因是
| ||
为了防止反应中生成的高温的熔融物炸裂集气瓶
为了防止反应中生成的高温的熔融物炸裂集气瓶
.(3)如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表.
| 气体发生装置内物质的总质量(g) | |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,反应中二氧化锰的作用是
| ||
催化作用
催化作用
.②反应生成氧气的质量为
0.8
0.8
g(结果精确到0.1g).(1)在实验室制取氧气和二氧化碳的装置中,可用同一个制取装置,写出此种制取氧气的化学方程式______为______反应类型.
(2)在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表
关于此反应,下列认识正确的是______
A.该变化的基本反应类型一定是置换反应
B.参加反应的甲、丙的质量比为1:9
C.乙、丁的相对分子质量比一定为10:9
D.甲反应后的质量为8g
(3)配平□FexOy+□CO═□Fe+□CO2 (填化学式前的计量数).
(4)在验证质量守恒定律的实验中,将打磨的铁钉放入到盛有硫酸铜的溶液中,过一段时间后,我们能观察到的现象是______其反应化学方程式为______.
查看习题详情和答案>>
(2)在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 4 | 1 | 42 | 10 |
| 反应前质量/g | 待测 | 20 | 6 | 31 |
A.该变化的基本反应类型一定是置换反应
B.参加反应的甲、丙的质量比为1:9
C.乙、丁的相对分子质量比一定为10:9
D.甲反应后的质量为8g
(3)配平□FexOy+□CO═□Fe+□CO2 (填化学式前的计量数).
(4)在验证质量守恒定律的实验中,将打磨的铁钉放入到盛有硫酸铜的溶液中,过一段时间后,我们能观察到的现象是______其反应化学方程式为______.
A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x是目前应用最广泛的金属,y常用作食品干燥剂.各物质间的转化关系如图所示(个别产物略去).
(1)B俗称
(2)F与G混合后遇明火可能发生
似的气体还有
(3)反应①的化学方程式为
(4)反应②的化学方程式为
(5)反应④的化学方程式是
查看习题详情和答案>>
(1)B俗称
熟石灰或消石灰
熟石灰或消石灰
;气体I的化学式为NH3
NH3
;
(2)F与G混合后遇明火可能发生
爆炸
爆炸
,与 F此性质相似的气体还有
CO(或CH4)
CO(或CH4)
.(3)反应①的化学方程式为
Fe+2HCl=FeCl2+H2↑
Fe+2HCl=FeCl2+H2↑
.(4)反应②的化学方程式为
CaCl2+Na2CO3═CaCO3↓+2NaCl
CaCl2+Na2CO3═CaCO3↓+2NaCl
.(5)反应④的化学方程式是
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
,实验现象是
| ||
剧烈燃烧,火星四射,放出热量,生成黑色固体
剧烈燃烧,火星四射,放出热量,生成黑色固体
.请回忆你学习过的“质量守恒定律”的实验探究.

(1)完成下面表格中的空格.
(2)方案一中白磷燃烧反应的化学方程式:
(3)由质量守恒定律可知,化学反应前后,一定不变的是
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类.
查看习题详情和答案>>

(1)完成下面表格中的空格.
| 实验方案 | 方案一 | 方案二 |
| 实验现象 | 天平平衡 天平平衡 |
天平平衡 |
| 反应前总质量(g) | 98.5 | 110.3 |
| 反应后总质量(g) | 98.5 | 110.3 110.3 |
| 实验结论分析 | 反应前总质量等于反应后总质量 反应前总质量等于反应后总质量 |
反应前总质量等于反应后总质量 |
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
;反应类型为
| ||
化合反应
化合反应
.(3)由质量守恒定律可知,化学反应前后,一定不变的是
①②⑤
①②⑤
(填序号)①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类.
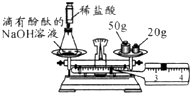 图是某班同学验证质量守恒定律实验的片段.
图是某班同学验证质量守恒定律实验的片段.(1)小佳用图示装置进行实验.反应前称得左盘内装置及物质总重量为
73.2
73.2
g,然后注入稀盐酸,充分反应后,能证明质量守恒定律的现象是天平仍保持平衡(或称量结果仍为73.2 g)
天平仍保持平衡(或称量结果仍为73.2 g)
;上述实验向氢氧化钠溶液中滴入酚酞的目的是验证稀盐酸与氢氧化钠溶液能发生化学反应(或指示中和反应是否完全反应)
验证稀盐酸与氢氧化钠溶液能发生化学反应(或指示中和反应是否完全反应)
;左盘中发生反应的化学方程式是HCl+NaOH═NaCl+H2O
HCl+NaOH═NaCl+H2O
.(2)小永向氢氧化钠溶液中注入稀盐酸,发现有气泡产生,其原因是
所用氢氧化钠溶液已与空气中二氧化碳反应生成了碳酸钠
所用氢氧化钠溶液已与空气中二氧化碳反应生成了碳酸钠
.