摘要:(3)ClO- + H2O HClO + OH-ClO- + Cl- +2 H+=== Cl2↑+ H2O
网址:http://m.1010jiajiao.com/timu_id_338055[举报]
(1)已知氯气与水的反应Cl2+H2O?HCl+HClO是一个可逆反应,即不能进行到底的反应,且反应生成的次氯酸(HClO)是一种酸性比碳酸还要弱的酸.分别写出盐酸、次氯酸的电离方程式:
(2)镁带着火时,不能用液态CO2灭火剂来灭火的原因是(用化学方程式表示)
(3)将少量铁粉投入到过量稀硝酸中发生反应的离子方程式是
查看习题详情和答案>>
HCl═H++Cl-
HCl═H++Cl-
、HClO?H++ClO-
HClO?H++ClO-
.(2)镁带着火时,不能用液态CO2灭火剂来灭火的原因是(用化学方程式表示)
2Mg+CO2
C+2MgO
| ||
2Mg+CO2
C+2MgO
.
| ||
(3)将少量铁粉投入到过量稀硝酸中发生反应的离子方程式是
略
略
,在此反应中,硝酸体现了氧化
氧化
性和酸
酸
性.实验室中制取氨的化学方程式为2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
| ||
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
用
| ||
向下排空气法
向下排空气法
法收集.下列离子方程式正确的是
将少量CO2气体通入NaClO溶液中;H+ + ClO- = HClO
在氯水中滴入少量NaOH溶液:Cl2 + 2OH- = Cl- + 2HClO
在Ca(HCO3)2溶液中滴入过量NaOH溶液:Ca2+ + HCO3- + OH-= CaCO3 ↓+ H2O
在AgF溶液中滴入盐酸:Ag+ + F- + H+ + Cl- = AgCl ↓+ HF
查看习题详情和答案>>下列离子方程式正确的是
A、将少量CO2气体通入NaClO溶液中;H+ + ClO- = HClO
B、 在氯水中滴入少量NaOH溶液:Cl2 + 2OH- = Cl- + 2HClO
C、 在Ca(HCO3)2溶液中滴入过量NaOH溶液:Ca2+ + HCO3- + OH-= CaCO3 ↓+ H2O
D、在AgF溶液中滴入盐酸:Ag+ + F- + H+ + Cl- = AgCl ↓+ HF
查看习题详情和答案>>
下列离子方程式正确的是
A、 将少量CO2气体通入NaClO溶液中;H+ + ClO- = HClO
B、 在氯水中滴入少量NaOH溶液:Cl2 + 2OH- = Cl- + 2HClO
C、 在Ca(HCO3)2溶液中滴入过量NaOH溶液:Ca2+ + HCO3- + OH-= CaCO3 ↓+ H2O
D、 在AgF溶液中滴入盐酸:Ag+ + F- + H+ + Cl- = AgCl ↓+ HF
查看习题详情和答案>>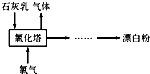 氯气是重要的化工原料.
氯气是重要的化工原料.(1)氯气溶于水得到氯水,氯水中存在下列反应:Cl2+H2O?H++Cl-+HClO,其平衡常数表达式为K=
| C(H+)C(Cl-)C(HClO) |
| C(Cl2) |
| C(H+)C(Cl-)C(HClO) |
| C(Cl2) |
(2)工业上常用消石灰和氯气反应制取漂白粉,化学反应方程式是
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
.流程如图所示,其主要设备是氯化塔,塔从上到下分四层.将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入,这样加料的目的是充分接触,充分反应
充分接触,充分反应
.处理从氯化塔中逸出气体的方法是用碱液来吸收
用碱液来吸收
.(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是
6OH-+3Cl2
ClO3-+5Cl-+3H2O
| ||
6OH-+3Cl2
ClO3-+5Cl-+3H2O
,其原因可能是
| ||
反应放热,温度升高,发生了副反应
反应放热,温度升高,发生了副反应
,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生.