摘要:(1)SO2 (g) +O2(g) SO3(g),△H – 98.3 kJ/mol (2)提高二氧化硫的转化率 因为该反应为放热反应.这样做是为了防止温度过高.而使SO2的转化率和催化剂的活性降低 (4)或× 100% (或通入盛有足量碱石灰的干燥管等.只要保证SO2和SO3不污染环境.SO3不与空气中的水接触的合理方案均可)
网址:http://m.1010jiajiao.com/timu_id_3248282[举报]
写出下列可逆反应的平衡常数(K)的表达式。
(1)SO2(g)+O2(g) SO3(g)______________;
SO3(g)______________;
(2)SiCl4(l)+2H2O(g) SiO2(s)+4HCl( g)_______________;
SiO2(s)+4HCl( g)_______________;
(3)2N2O5(g) 4NO2(g)+O2(g)______________ ;
4NO2(g)+O2(g)______________ ;
(4)3Fe(s) +4H2O(g) Fe3O4(s)+4H2(g)______________ 。
Fe3O4(s)+4H2(g)______________ 。
查看习题详情和答案>>
(1)SO2(g)+O2(g)
 SO3(g)______________;
SO3(g)______________;(2)SiCl4(l)+2H2O(g)
 SiO2(s)+4HCl( g)_______________;
SiO2(s)+4HCl( g)_______________; (3)2N2O5(g)
 4NO2(g)+O2(g)______________ ;
4NO2(g)+O2(g)______________ ; (4)3Fe(s) +4H2O(g)
 Fe3O4(s)+4H2(g)______________ 。
Fe3O4(s)+4H2(g)______________ 。 某同学想通过利用下图所示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物.
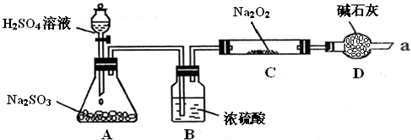
实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g.请分析:
Ⅰ.装置B的作用
Ⅱ.如何检验反应中是否有O2生成
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:
(1)若按假设2进行,反应方程式为
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4.
该方案是否合理
(3)若假设1成立,某同学以反应前后C管的质量差( m 2-m 1 )g为依据推断生成Na2SO3的质量为( m 2-m 1 )×126/64g.老师提示推算不合理,请你分析其中的缘由:
(4)若假设2成立,则参加反应的Na2O2物质的量为
(列计算式)摩尔.
查看习题详情和答案>>

实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g.请分析:
Ⅰ.装置B的作用
干燥SO2气体,防止水蒸气与Na2O2反应
干燥SO2气体,防止水蒸气与Na2O2反应
.装置D的作用防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应,同时吸收过量的SO2,以免污染空气
防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应,同时吸收过量的SO2,以免污染空气
.Ⅱ.如何检验反应中是否有O2生成
用带火星的木条靠近干燥管口a,观察其是否燃烧
用带火星的木条靠近干燥管口a,观察其是否燃烧
.Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:
有Na2SO3和Na2SO4
有Na2SO3和Na2SO4
.(1)若按假设2进行,反应方程式为
Na2O2+SO2=Na2SO4
Na2O2+SO2=Na2SO4
.(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4.
该方案是否合理
否
否
(填“是”或“否”),理由是HNO3有氧化性,据此不能确定产物是Na2SO3还是Na2SO4或二者兼有
HNO3有氧化性,据此不能确定产物是Na2SO3还是Na2SO4或二者兼有
.(3)若假设1成立,某同学以反应前后C管的质量差( m 2-m 1 )g为依据推断生成Na2SO3的质量为( m 2-m 1 )×126/64g.老师提示推算不合理,请你分析其中的缘由:
因为该反应中吸收SO2同时有O2产生,所以(m2-m1)不等于参加反应的SO2质量,故该推算不合理
因为该反应中吸收SO2同时有O2产生,所以(m2-m1)不等于参加反应的SO2质量,故该推算不合理
.(4)若假设2成立,则参加反应的Na2O2物质的量为
| m2-m1 |
| 64 |
| m2-m1 |
| 64 |
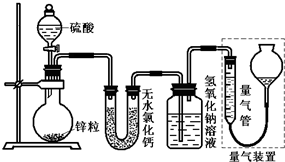 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10l kPa,温度为0℃).
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10l kPa,温度为0℃).(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是
A.200mL B.400mL C.500mL
(2)某同学认为:若1.30g锌粒完全溶解,只要测得氢氧化钠溶液洗气瓶增重l.28g,就可确定圆底烧瓶中发生反应的化学方程式为:
(3)若向烧瓶中加入a g锌,同时向烧瓶中加入了V1 ml浓硫酸,且锌完全反应,氢氧化钠洗气瓶增重b g.量气管中收集到V2ml气体,则有:a g/65g?mol-1=b g/64g?mol-1+(V2-V1)ml/22400ml?mol-1,依据的原理是
(4)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重m g,则整个实验过程产生的气体中,n(H2)/n(SO2)=
(5)反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
①