摘要:14.氯化铜晶体(CuCl2·xH2O)是重要的化工原料.可用作反应的催化剂.消毒剂等.用孔雀石[主要含Cu2(OH)2CO3.还含少量Fe.Si的化合物]制备氯化铜晶体.方案如下: 已知:Ⅰ.Cu(OH)2.CuO开始分解的温度分别为80℃和900℃. Ⅱ.有关金属离子从开始沉淀到沉淀完全时溶液的pH: 开始沉淀的pH 沉淀完全的pH Fe3 2.7 3.7 Cu2+ 5.2 6.4 Fe2+ 7.6 9.6 (1)若溶液A含有的金属离子有Cu2+.Fe2+.Fe3+.则试剂①最好为 . a.(NH4) 2S b.H2O2 c.NaClO d.Cl2 (2)加试剂②的目的是 .由溶液C获得CuCl2·xH2O.需要经过加热浓缩. .过滤等操作. (3)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值.有如下两种实验方案: 方案一:称取a g晶体灼烧至质量不再减轻为止.冷却.称量所得无水CuCl2的 质量为b g. 方案二:称取a g晶体.加入足量氢氧化钠溶液.过滤.洗涤.加热沉淀至质量不再减轻为止.称量所得固体的质量为b g. 则上述两种实验方案中.不合理的是 .原因是 . 依据合理方案计算得x = (用含a.b的代数式表示).
网址:http://m.1010jiajiao.com/timu_id_3241720[举报]
氯化铜晶体(CuCl2·xH2O)是重要的化工原料,可用作反应的催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
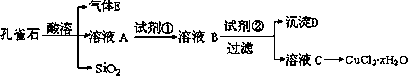
已知:Ⅰ.Cu(OH)2、CuO开始分解的温度分别为80℃和900℃.
Ⅱ.有关金属离子从开始沉淀到沉淀完全时溶液的pH:
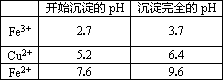
(1)若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①最好为________(填字母).
a.(NH4)2S
b.H2O2
c.NaClO
d.Cl2
(2)加试剂②的目的是________,由溶液C获得CuCl2·xH2O,需要经过加热浓缩、________、过滤等操作.
(3)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,有如下两种实验方案:
方案一:称取a g晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的
质量为b g.
方案二:称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀(控制温度约为120℃)至质量不再减轻为止,称量所得固体的质量为bg.
则上述方案中不合理的是________,原因是________.
依据合理方案计算得x=________(用含a、b的代数式表示).
氯化铜晶体(CuCl2?xH2O)是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
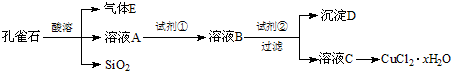
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
(1)若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①选用
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是
(3)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x=
(用含a、b的代数式表示).
查看习题详情和答案>>

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
B
B
(填字母).A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是
3.7~5.4
3.7~5.4
.由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是蒸发浓缩
蒸发浓缩
、冷却结晶
冷却结晶
过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是防止CuCl2?xH2O晶体溶解损失
防止CuCl2?xH2O晶体溶解损失
.(3)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是
CuCl2?xH2O晶体加热时会发生水解
CuCl2?xH2O晶体加热时会发生水解
.②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x=
| 80a-135b |
| 18b |
| 80a-135b |
| 18b |
氯化铜晶体(CuCl2?xH2O)是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是______.由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是______、______过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是______.
(3)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是______.
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x=______(用含a、b的代数式表示). 查看习题详情和答案>>
氯化铜晶体(CuCl2?xH2O)是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
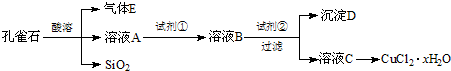
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
(1)若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①选用______(填字母).
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是______.由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是______、______过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是______.
(3)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是______.
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x=______(用含a、b的代数式表示).
查看习题详情和答案>>

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是______.由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是______、______过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是______.
(3)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是______.
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x=______(用含a、b的代数式表示).
氯化铜晶体是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
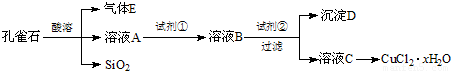
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
(1)若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①选用 (填字母).
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是 .由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是 、 过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是 .
(3)为了测定制得的氯化铜晶体中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是 .
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x= (用含a、b的代数式表示). 查看习题详情和答案>>

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是 .由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是 、 过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是 .
(3)为了测定制得的氯化铜晶体中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是 .
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x= (用含a、b的代数式表示). 查看习题详情和答案>>