摘要:23.解析:
网址:http://m.1010jiajiao.com/timu_id_3219478[举报]
| Ⅰ:下列有关实验的描述不正确的是____(填序号); ①用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准溶液润洗,则测定结果偏低。 ② 配制一定物质的量浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高; ③ 将Fe2(SO4)3溶液加热蒸发至干并灼烧,最后得到红棕色粉末 ④ 硝酸钾过饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出。 ⑤可用25ml酸式滴定管量取20.00mlKMnO4溶液 ⑥分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多 Ⅱ:三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通 过实验来探究红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下: 查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。 提出假设 假设1:红色粉末是Fe2O3 假设2:红色粉末是Cu2O 假设3:红色粉末是Fe2O3和Cu2O的混合物 设计探究实验 取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。 (1)若假设1成立,则实验现象是_________________。 (2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?_________________。简述你的理由(不需写出反应的方程式)___________________。 (3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是____________,写出发生反应的离子方程式________________。 探究延伸 经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。 (4)实验小组欲用加热法测定Cu2O的质量分数。取ag固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为________。 (5)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下: | ||||||||||||
| ||||||||||||
| 实验室有下列试剂可供选择: A、氯水 B、H2O2 C、NaOH D、Cu2(OH)2CO3 实验小组设计如下方案 | ||||||||||||
 | ||||||||||||
| 试回答: ①试剂1为_______,试剂2为________(填字母)。 ②固体X的化学式为____________。 ③操作I为___________。 |
【解析】A项电荷守恒等式为:c(H+)+c(Na+)=c(OH-)+c(HSO3-)+c(HCO3-)+2c(CO32-) +2c(SO32-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(HSO3-)+c(HCO3-)+2c(CO32-)+2c(SO32-),A项不正确。
B项中的电荷守恒式为:c(Na+)+c(H+)=c(Cl-)+c(CH3COO-)+c(OH-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(Cl-)+c(CH3COO-);根据物料守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),由此二式导出c(Cl-)=c(CH3COOH),综上所述,有c(Na+)>c(Cl-)=c(CH3COOH),B项不对
C项中,NH4+水解呈酸性,CO32-水解呈碱性,它促进NH4+的水解;Fe2+水解呈酸性,它抑制NH4+的水解,所以三种溶液中c(NH4+):③>②>①,C项正确。
D项中,盐类的水解促进水的电离,强酸和弱酸都会抑制水的电离,当c(H+)相同时,对水的电离产生的抑制作用相同,正确的顺序应为①>②=③,D项不对。
【答案】C
查看习题详情和答案>>为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇.“绿色自由”构想的部分技术流程如下:
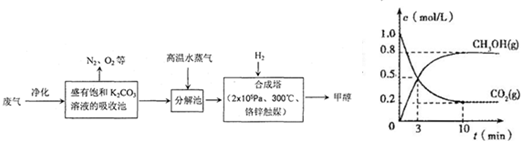
(1)合成塔中反应的化学方程式为
(2)从合成塔分离出甲醇的原理与下列
A.过滤 B.分液 C.蒸馏 D.结晶
(3)工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施.“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括
(4)在体积为2L的合成塔中,充入2mol CO2和6mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.从反应开始到平衡,v(H2)=
(5)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3kJ/mol,H2 (g)+
O2(g)=H2O(l)△H2=-285.8kJ/mol写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式
查看习题详情和答案>>

(1)合成塔中反应的化学方程式为
CO2+3H2
→CH3OH+H2O
| 一定条件 |
CO2+3H2
→CH3OH+H2O
;△H<0.从平衡移动原理分析,低温有利于提高原料气的平衡转化率.而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了| 一定条件 |
催化剂的催化活性
催化剂的催化活性
.(2)从合成塔分离出甲醇的原理与下列
C
C
操作的原理比较相符(填字母).A.过滤 B.分液 C.蒸馏 D.结晶
(3)工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施.“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括
高温水蒸气
高温水蒸气
.(4)在体积为2L的合成塔中,充入2mol CO2和6mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.从反应开始到平衡,v(H2)=
0.24mol/(L?min)
0.24mol/(L?min)
;能使平衡体系中n(CH3OH)/n(CO2)增大的措施有增大H2的用量等
增大H2的用量等
.(5)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3kJ/mol,H2 (g)+
| 1 |
| 2 |
CO2(g)+4H2(g)=CH4(g)+2H2O(l)△H=-252.9kJ/mol
CO2(g)+4H2(g)=CH4(g)+2H2O(l)△H=-252.9kJ/mol
.分析比较:
(1)绿色食品;白色污染;赤潮;蓝矾.与颜色有关的物质是
(2).Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
(3)处于下列状态的物质中不能导电但属于电解质的有:
A.氯化钠晶体 B.干冰 C.冰醋酸 D.铜 E.硫酸钡晶体 F.蔗糖 G.酒精 H.熔融的硝酸钾 J.氯化氢气体 K.氢氧化钠溶液.
查看习题详情和答案>>
(1)绿色食品;白色污染;赤潮;蓝矾.与颜色有关的物质是
白色污染、赤潮、蓝矾
白色污染、赤潮、蓝矾
(2).Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
分散质微粒直径大小在1~100nm之间
分散质微粒直径大小在1~100nm之间
.(填:丁达尔效应、微粒直径大小在1~100nm之间、均一的分散系、电泳、聚沉、分散质能通过滤纸、)(3)处于下列状态的物质中不能导电但属于电解质的有:
J
J
填序号).A.氯化钠晶体 B.干冰 C.冰醋酸 D.铜 E.硫酸钡晶体 F.蔗糖 G.酒精 H.熔融的硝酸钾 J.氯化氢气体 K.氢氧化钠溶液.
分析、归纳、探究是学习化学的重要方法和手段之一.下面就电解质A回答有关问题(假定以下都是室温时的溶液).
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a.
①当a=10时,A溶液呈碱性的原因是(用离子方式程式表示)
②当a=10,n=1时,A溶液中各种离子浓度由大到小的顺序为
当a=11,n=2时,A溶液中各种离子浓度由大到小的顺序为
③当n=1、c=0.1,溶液中c(HB):c(B-)=1:99时,A溶液的pH为
(2)已知难溶电解质A的化学式为X2Y3,测得其饱和溶液中X3+离子的浓度为c mol/L,则该难溶物X2Y3的溶度积常数为Ksp=
c5
c5.
查看习题详情和答案>>
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a.
①当a=10时,A溶液呈碱性的原因是(用离子方式程式表示)
Bn-+H2O?HB(n-1)-+OH-
Bn-+H2O?HB(n-1)-+OH-
.②当a=10,n=1时,A溶液中各种离子浓度由大到小的顺序为
c(Na+)>c(B-)>c(OH-)>c(H+)
c(Na+)>c(B-)>c(OH-)>c(H+)
,c(OH-)-c(HB)=1×10-10
1×10-10
mol/L.当a=11,n=2时,A溶液中各种离子浓度由大到小的顺序为
c(Na+)>c(HB-)>c(OH-)>c(H+)>c(B2-)
c(Na+)>c(HB-)>c(OH-)>c(H+)>c(B2-)
,当a=9,n=2时,NaHB的溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HB-)>c(OH-)>c(H+)>c(B2-)
c(Na+)>c(HB-)>c(OH-)>c(H+)>c(B2-)
,当a=6,n=2时,NaHB溶液呈酸性的原因是(用离子方式程式表示)HB-+H2O?B2-+H3O+
HB-+H2O?B2-+H3O+
,NaHB的溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HB-)>c(H+)>c(B2-)>c(OH-)
c(Na+)>c(HB-)>c(H+)>c(B2-)>c(OH-)
.③当n=1、c=0.1,溶液中c(HB):c(B-)=1:99时,A溶液的pH为
11
11
(保留整数值).(2)已知难溶电解质A的化学式为X2Y3,测得其饱和溶液中X3+离子的浓度为c mol/L,则该难溶物X2Y3的溶度积常数为Ksp=
| 27 |
| 8 |
| 27 |
| 8 |