网址:http://m.1010jiajiao.com/timu_id_3210720[举报]

(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是
| Cu |
| △ |
| Cu |
| △ |
①向试管中滴入3滴乙醛溶液.②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止.③振荡后
(3)某实验小组取用实验室的乙醛溶液进行银镜实验未能成功,查阅资料发现乙醛分子间易形成加合物(C2H4O)n而不能发生银镜,加合物(C2H4O)n不能发生银镜反应的原因


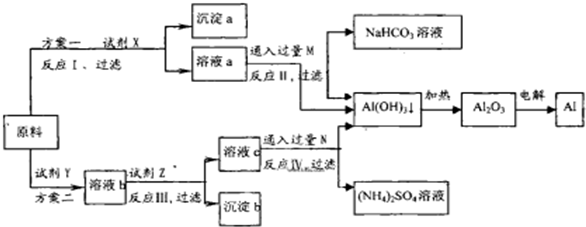
(1)试剂X的化学式为
实验室配制480mL 1mol?L-1 X的溶液必须用到玻璃仪器除烧杯、玻璃棒、试剂瓶、胶头滴管外,还有
(2)按照方案设计,试剂Z的作用是调节溶液的pH,以生成沉淀b[Fe(OH)3].从实际工业的角度,你认为方案
(3)已知N为氨气,实验室中还可以用下图装置制取氨气并进行氨气喷泉实验.
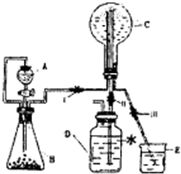
①仪器A的名称是
②若用此装置制备N气,若A中盛有浓氨水,则B装置中的固体试剂不可以选用下列的
A.生石灰 B.烧碱 C.胆矾 D.碱石灰
(4)若D中事先滴入少量酚酞,则C中液体呈
若X、Y两种元素在周期表中位于同一主族,其中一种为短周期元素,且两者相隔一个周期,并有m=n>0。在一定条件下有下列反应(未配平):
Xm + Yn + H2O → HXO3 + HY。请回答:
⑴该反应的还原剂的电子式为___________________。
⑵配平上述化学方程式(用化学式表示):
⑶若某化学反应如下:(未配平)KX + Yn + H2O → KXO3 + Xm + HY + KY
若KXO3和Xm的化学计量数均为1,则Yn的化学计量数为____________。
在下面化学式上标出电子转移的方向和数目:
KX + Yn + H2O →
⑷已知:在反应中,若氧化反应和还原反应发生在同一分子内部处于同一化合价的同种元素上,使该元素的原子(或离子)一部分被氧化,另一部分被还原。这种自身的氧化还原反应称为歧化反应。实验室模拟KXO3的制法如下:
①在进行步骤Ⅰ实验时,有学生主张电解装置用U形管,有的学生主张用烧杯,你认为用哪种仪器更合适______________(填名称)。
②步骤Ⅰ的阴极电极反应式为(用化学式表示):_____________________。
③步骤Ⅰ中由NaYO歧化生成NaYO3的离子方程式为(用化学式表示):______________________。
④步骤Ⅱ中向NaYO3的溶液中加入粉末状的KY,搅拌后生成KYO3。在2L 3 mol·L-1的NaYO3溶液,则至少需要加入__________mol KY粉末可将溶液中的YO3-离子沉淀至浓度变为0.1 mol·L-1。[已知Ksp(KYO3)= 0.366,计算结果保留两位小数,加入KY粉末后溶液体积不变]
查看习题详情和答案>>
实验事实:某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中结果得到蓝色沉淀。
Ι.甲同学认为:CuCO3是难溶解的物质,两者反应只有CuCO3一种沉淀生成;
乙同学认为: CO32-和Cu2+两者相互促进,发生水解反应,只生成Cu(OH)2一种沉淀;
丙同学认为:两种因素都有存在,应生成CuCO3和Cu(OH)2两种沉淀。
[查阅资料知:CuCO3和Cu(OH)2均不带结晶水].用离子方程式表示甲乙同学的观点
甲同学
乙同学
Ⅱ.在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为:①过滤②洗涤③干燥。
过滤除了使用铁架台、玻璃棒、烧杯外,还要用到的玻璃仪器是:_______;洗涤后的沉淀应____(选填下列序号)干燥:
A.在干燥管中 B.在U型管中 C.在干燥器中 D.在装有浓硫酸的洗气瓶中 E.在坩埚中微热
Ⅲ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。

各装置连接顺序为A →C→B。装置C中装有试剂无水硫酸铜,若C中无水硫酸铜变蓝,澄清石灰水变浑浊,说明生成的沉淀的成分是: (写化学式)。
Ⅳ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。

⑴各装置的仪器连接顺序是 (按照气体流向从左往右用字母表示)。
⑵ 若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为: (只列计算式)。
查看习题详情和答案>>
若X、Y两种元素在周期表中位于同一主族,其中一种为短周期元素,且两者相隔一个周期,并有m=n>0。在一定条件下有下列反应(未配平):
Xm + Yn + H2O → HXO3 + HY。请回答:
⑴该反应的还原剂的电子式为___________________。
⑵配平上述化学方程式(用化学式表示):
⑶若某化学反应如下:(未配平)KX + Yn + H2O → KXO3 + Xm + HY + KY
若KXO3和Xm的化学计量数均为1,则Yn的化学计量数为____________。
在下面化学式上标出电子转移的方向和数目:
KX + Yn + H2O →
⑷已知:在反应中,若氧化反应和还原反应发生在同一分子内部处于同一化合价的同种元素上,使该元素的原子(或离子)一部分被氧化,另一部分被还原。这种自身的氧化还原反应称为歧化反应。实验室模拟KXO3的制法如下:
①在进行步骤Ⅰ实验时,有学生主张电解装置用U形管,有的学生主张用烧杯,你认为用哪种仪器更合适______________(填名称)。
②步骤Ⅰ的阴极电极反应式为(用化学式表示):_____________________。
③步骤Ⅰ中由NaYO歧化生成NaYO3的离子方程式为(用化学式表示):______________________。
④步骤Ⅱ中向NaYO3的溶液中加入粉末状的KY,搅拌后生成KYO3。在2L 3 mol·L-1的NaYO3溶液,则至少需要加入__________mol KY粉末可将溶液中的YO3-离子沉淀至浓度变为0.1 mol·L-1。[已知Ksp(KYO3)= 0.366,计算结果保留两位小数,加入KY粉末后溶液体积不变]