摘要:构成原子的各粒子间的关系.有时结合阿伏伽德罗常数.氧化还原反应来进行考察.如“氯气发生氧化还原反应时.1摩尔氯气一定得到2摩尔电子 .很多学生没有考虑到氯气还可能发生自身氧化还原反应.还如铜与硫反应时生成的是硫化亚铜而不是硫化铜.要求考生在平时的练习中要注意总结.
网址:http://m.1010jiajiao.com/timu_id_3199473[举报]
由短周期元素形成的六种微粒,有4种离子,两种分子,其中A、F是由非金属元素的原子构成的阳离子,这六种微粒均具有10个电子,它们间的相互关系如下:
a.A、B两种离子在加热条件下,可生成C、D两种分子
b.C是常温下呈气态的分子,遇Cl2时可冒白烟
c.E、B两种离子相互作用可生成2个D的分子
d.含F微粒的溶液,遇B会产生白色沉淀W、B过量时,W又可溶解变为无色溶液;在此无色溶液中加入E时,又产生白色沉淀W,E过量时,W又转化为F.
根据以上事实,回答以下各问:
(1)写出A+B![]() C+D的化学方程式
C+D的化学方程式
________________________
(2)C遇Cl2冒白烟的化学方程式是
________________________
(3)写出E、B反应生成2D的离子方程式
________________________
(4)F微粒的符号是________,白色沉淀W的化学式是________W溶于B的产物与E又生成W的离子方程式是________
查看习题详情和答案>>已知a、I、e为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
| 粒子代码 | a | I | e |
| 原子核数 | 单核 | 四核 | 双核 |
| 粒子的电荷数 | 一个单位正电荷 | 0 | 一个单位负电荷 |

请填写下列空白:?
(1)写出下列物质的化学式:B J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。?②I溶于G 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为 。 查看习题详情和答案>>
已知a、e、I为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
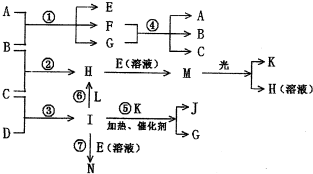
物质A由a、e构成,B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①-⑤都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去.
请填写下列空白:
(1)a的结构示意图:
 J分子的极性
J分子的极性
(2)写出下列反应的离子反应方程式:
H+E(溶液)→M
(3)E(溶液)能与I以1:2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出该反应的化学方程式
(4)L是由3种元素构成的分子,能与I以1:2的物质的量之比反应生成尿素CO(NH2)2和物质H,写出L的电子式
 ;
;
(5)反应③用于工业生产时应在
所使用的一种特殊材料的名称为
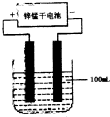
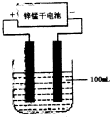
(6)常温下,实验室模拟工业反应④的过程如图所示,标况下,当电极上产生 112ml(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=
查看习题详情和答案>>

物质A由a、e构成,B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①-⑤都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去.
请填写下列空白:

(1)a的结构示意图:


极性分子
极性分子
,在F的晶体中,与a离子距离最近且相等的a离子个数为12
12
个.(2)写出下列反应的离子反应方程式:
H+E(溶液)→M
H++ClO-═HClO
H++ClO-═HClO
,F+G→A+B+C2Cl-+2H2O
2OH-+Cl2↑+H2↑
| ||
2Cl-+2H2O
2OH-+Cl2↑+H2↑
.
| ||
(3)E(溶液)能与I以1:2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出该反应的化学方程式
NaClO+2NH3═N2H4+NaCl+H2O
NaClO+2NH3═N2H4+NaCl+H2O
(4)L是由3种元素构成的分子,能与I以1:2的物质的量之比反应生成尿素CO(NH2)2和物质H,写出L的电子式


(5)反应③用于工业生产时应在
合成塔
合成塔
中进行(填设备名称);反应④用于工业生产时为了防止B和C混合反应产生危险,所使用的一种特殊材料的名称为
离子交换膜
离子交换膜
,在该工业生产中它还具有的作用是只允许阴离子和气体通过从而防止NaOH与氯气反应
只允许阴离子和气体通过从而防止NaOH与氯气反应
.(6)常温下,实验室模拟工业反应④的过程如图所示,标况下,当电极上产生 112ml(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=
13
13
.(假设气体完全逸出,溶液体积不变),此时锌锰干电池中消耗锌0.325
0.325
克.
已知a、e、I为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
物质A由a、e构成,B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①-⑤都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去.
请填写下列空白:
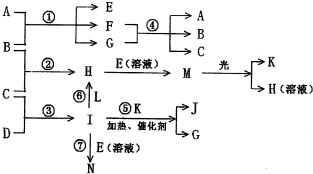
(1)a的结构示意图:______J分子的极性______,在F的晶体中,与a离子距离最近且相等的a离子个数为______个.
(2)写出下列反应的离子反应方程式:
H+E(溶液)→M______,F+G→A+B+C______.
(3)E(溶液)能与I以1:2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出该反应的化学方程式______
(4)L是由3种元素构成的分子,能与I以1:2的物质的量之比反应生成尿素CO(NH2)2和物质H,写出L的电子式______;
(5)反应③用于工业生产时应在______中进行(填设备名称);反应④用于工业生产时为了防止B和C混合反应产生危险,
所使用的一种特殊材料的名称为______,在该工业生产中它还具有的作用是______.
(6)常温下,实验室模拟工业反应④的过程如图所示,标况下,当电极上产生 112ml(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=______.(假设气体完全逸出,溶液体积不变),此时锌锰干电池中消耗锌______克.
查看习题详情和答案>>
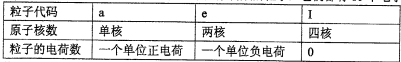
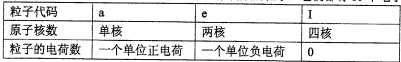
已知a、e、I为三种由短周期元素构成的10个电子的粒子,其结构特点如下:
| 粒子代码 | a | e | I |
| 原子核数 | 单核 | 两核 | 四核 |
| 粒子的电荷数 | 一个单位正电荷 | 一个单位负电荷 | 0 |

(1)写出下列物质的化学式:B______,J______.
(2)写出下列反应的离子反应方程式:H+E(溶液)→M______,F+G→A+B+C______;
(3)E(溶液)能与I以1:2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出N的结构式______;
(4)L是由3种元素构成的分子,能与I以1:2的物质的量之比反应生成尿素CO(NH2)2和物质H,写出L
 的电子式______;
的电子式______;(5)常温下,实验室模拟工业反应④的过程如图所示,标况下,当电极上产生112mL(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=______.(假设气体完全逸出,溶液体积不变) 查看习题详情和答案>>