摘要:R-H R - A 烃 烃的衍生物 A可为:-X.-OH.-CHO.-COOH.-COOR′.-NO2.-NH2等 (2)重要的烃的衍生物: (1)卤代烃:R-X(饱和一元卤代烃通式:CnH2n+1X,代表物:CH3CH2Br) (2)醇:R-OH(饱和一元醇通式:CnH2n+2O,代表物:CH3CH2OH) (3)酚:代表物 (4)醛:R-CHO(代表物:CH3CHO.HCHO) (5)羧酸:RCOOH(代表物CH3COOH) (6)酯:R-COOR′(代表物CH3COOC2H5) (3)重要性质 (1)分析基本化学方程式断键情况.理解反应简单机理和官能团性质. (2)转化关系: (3)烃的衍生物的比较 类别 官能团 分子结构特点 分 类 主要化学性质 卤 代 烃 卤原子(-X) 碳-卤键(C-X)有极性.易断裂 ①氟烃.氯烃.溴烃,②一卤烃和多卤烃,③饱和卤烃.不炮和卤烃和芳香卤烃 ①取代反应: R-X+H2O R-OH + HX ②消去反应:R-CH2-CH2X + NaOH RCH=H2 + NaX + H2O 醇 均为羟基 (-OH) -OH在非苯环碳原子上 ①脂肪醇,②脂环醇③芳香醇.④一元醇与多元醇 ①取代反应: a.与Na等活泼金属反应,b.与HX反应.c.分子间脱水,d.酯化反应 ②氧化反应: 2R-CH2OH + O2 2R-CHO+2H2O ③消去反应. CH3CH2OH CH2=H2↑+ H2O 酚 -OH直接连在苯环碳原上.酚类中均含苯的结构 一元酚.二元酚.三元酚等 ①易被空气氧化而变质,②具有弱酸性③取代反应 ④显色反应 醛 醛基 分子中含有醛基的有机物 ①脂肪醛,②芳香醛,③一元醛与多元醛 ①加成反应(与H2加成又叫做还原反应):R-CHO+H2R-CH2OH ②氧化反应:a.银镜反应,b.红色沉淀反应:c.在一定条件下.被空气氧化 羧酸 羧基 分子中含有羧基的有机物 ①脂肪酸与芳香酸,②一元酸与多元酸,③饱和羧酸与不饱和羧酸,④低级脂肪酸与高级脂肪酸 ①具有酸的通性,②酯化反应 羧 酸 酯 酯基 (R为烃基或H 原子.R′只能为烃基) ①饱和一元酯: CnH2n+lCOOCmH2m+1 ②高级脂肪酸甘油酯③聚酯④环酯 水解反应:RCOOR′+ H2ORCOOH + R'OH RCOOR′+ NaOH RCOONa + R'OH
网址:http://m.1010jiajiao.com/timu_id_3199446[举报]
 如图是表示:2X+Y?Z+R△H<0 的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是( )
如图是表示:2X+Y?Z+R△H<0 的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是( )| A、减少Z物质 | B、加大压强 | C、升高温度 | D、使用催化剂 |
|
归纳总结是学习与研究化学行之有效的方法,某同学在全面复习的基础上作出如下归纳: ①固体的热稳定性:Na2CO3>CaCO3>NaHCO3 ②给出质子能力:CH3COOH>CH3CH2OH>H2O ③相同物质的量浓度溶液中c(NH4+):(NH4)2SO4>(NH4)2CO3>NH4Cl ④微粒半径:r(H+)>r(H)>r(H-) ⑤熔沸点:H2O>H2S>H2Se ⑥不活泼金属单质一定不能与活泼金属盐溶液反应 以上归纳中正确的是 | |
| [ ] | |
A. |
①② |
B. |
③④ |
C. |
①③ |
D. |
②⑥ |
(1)AgNO3的水溶液呈
(2)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所至;乙同学认为是溶液中Na2CO3电离出的CO32-水解所至.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化
如右图所示.则图中表示醋酸溶液中pH变化曲线的是
(选填“<”、“=”、“>”)
(4)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一.
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:负极:
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸 门上的固体材料R可以采用
门上的固体材料R可以采用
A.铜 B.钠
C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
(5)氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
①氢氧燃料电池的能量转化主要形式是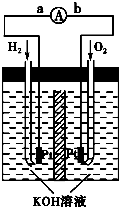 方向为
方向为
②负极反应式为
③电极表面镀铂粉的原因为
查看习题详情和答案>>
酸
酸
(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):Ag++H2O  AgOH+H+
AgOH+H+
 AgOH+H+
AgOH+H+Ag++H2O  AgOH+H+
AgOH+H+
;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的 AgOH+H+
AgOH+H+硝酸
硝酸
中,然后再用蒸馏水稀释到所需的浓度.若用惰性电极电解AgNO3的水溶液,请写出电池反应的离子方程式4Ag++2H2O
4Ag+O2↑+4H+
| ||
4Ag++2H2O
4Ag+O2↑+4H+
,
| ||
(2)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所至;乙同学认为是溶液中Na2CO3电离出的CO32-水解所至.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
向红色溶液中加入足量BaCl2溶液
向红色溶液中加入足量BaCl2溶液
如果溶液还显红色说明甲正确,红色褪去说明乙正确
如果溶液还显红色说明甲正确,红色褪去说明乙正确
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化

如右图所示.则图中表示醋酸溶液中pH变化曲线的是
B
B
(填“A”或“B”).设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2.则m1<
<
m2(选填“<”、“=”、“>”)
(4)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一.
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:负极:
2Fe=2Fe2++4e-
2Fe=2Fe2++4e-
正极:O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
;②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸
 门上的固体材料R可以采用
门上的固体材料R可以采用C
C
.A.铜 B.钠
C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
负
负
极.(5)氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
①氢氧燃料电池的能量转化主要形式是
化学能转变为电能
化学能转变为电能
,在导线中电子流动 方向为
方向为a→b
a→b
(用a、b表示).②负极反应式为
2H2+4OH-=4H2O+4e-
2H2+4OH-=4H2O+4e-
.③电极表面镀铂粉的原因为
增大电极单位面积吸附H2、O2分子数,加快电极反应速率
增大电极单位面积吸附H2、O2分子数,加快电极反应速率
. 如图是表示:2X+Y?Z+R△H<0的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是( )
如图是表示:2X+Y?Z+R△H<0的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是( )