摘要:(1)12×3+1×6+14×6==126 (2)C∶O∶N==36∶6∶84==6∶1∶14 (3)三聚氰胺中氮元素的质量分数==84/126==66.7% 解析:根据化学式进行计算.求化合物中各元素的质量比.须指明是哪种元素之间的质量比,化合物中某元素的质量分数.算式中分母是化合物的相对分子质量.分子是该元素的相对原子质量乖以该元素的原子个数.相对分子质量是化学式中各原子的相对原子质量之和.元素的质量比是各元素的“相对原子质量×原子个数 之比.元素的质量分数是该元素的“相对原子质量×原子个数 除以相对分子质量. 变式训练二
网址:http://m.1010jiajiao.com/timu_id_3191568[举报]
乳酸(C3H6O3)是一种重要的体内代谢物.
(1)某同学计算乳酸的相对分子质量为12+1+16=29,这是错误的.请你帮他改正为
(2)每个乳酸分子中碳、氢、氧的原子个数比为
(3)180g乳酸中的碳元素与
查看习题详情和答案>>
(1)某同学计算乳酸的相对分子质量为12+1+16=29,这是错误的.请你帮他改正为
12×3+1×6+16×3=90
12×3+1×6+16×3=90
;(2)每个乳酸分子中碳、氢、氧的原子个数比为
1:2:1
1:2:1
;(3)180g乳酸中的碳元素与
180
180
g葡萄糖(C6H12O6)中的碳元素质量相等.
如图所示,A为无色、无刺激性气味的气体,装置Ⅰ中硬质玻璃管中有1.60克红色粉末B,且A、B均为纯净物,实验情况如下表所示:
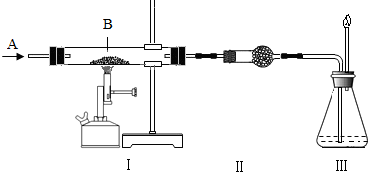
(1)将所得黑色粉末加入足量的稀硫酸中,可生成0.04克氢气,同时生成一种化合物RSO4.则通过计算可确定金属R的相对原子质量为 .
(2)试描述上述黑色粉末与稀硫酸反应的现象 .
(3)将符合组分装置设计图的标号填写在横线上 .
①说明了A具有还原性 ②说明了A具有可燃性 ③说明A得氧后的产物是CO2 ④有效地防止了A扩散到空气中. 查看习题详情和答案>>

| 实验内容 | 实验现象 | 测量结果 |
| (1)使A持续通过装置Ⅰ、Ⅱ、Ⅲ | Ⅰ中B全变为黑色 | 黑色粉末为1.12克 |
| (2)当A与B在加热反应时 | Ⅱ中干燥管里的无水硫酸铜无变化 | |
| (3)实验结束 | Ⅲ中石灰水变浑浊 | Ⅲ中有1克沉淀 |
(2)试描述上述黑色粉末与稀硫酸反应的现象
(3)将符合组分装置设计图的标号填写在横线上
①说明了A具有还原性 ②说明了A具有可燃性 ③说明A得氧后的产物是CO2 ④有效地防止了A扩散到空气中. 查看习题详情和答案>>
下表是3种物质在不同温度时的溶解度,根据表格信息答题.
(1)某饱和溶液随温度升高有固体析出,则该饱和溶液的溶质是 (填化学式).
(2)在40℃时,S(NaCl) S(KNO3)(填写“>”、“<”或“=”).
(3)要配制20℃时的NaCl饱和溶液100g,需要NaCl的质量为 g(保留小数点后一位).
(4)某KNO3晶体中有少量NaCl杂质,要得到纯净KNO3的方法是:先加热溶解,然后
,过滤、洗涤、干燥后得到KNO3晶体.
查看习题详情和答案>>
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
| Ca(OH)2 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 | |
(2)在40℃时,S(NaCl)
(3)要配制20℃时的NaCl饱和溶液100g,需要NaCl的质量为
(4)某KNO3晶体中有少量NaCl杂质,要得到纯净KNO3的方法是:先加热溶解,然后
追踪科学家的足迹
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI.
材料2:四种盐在不同温度下的溶解度表.
试回答下列问题:
(1)在实验室中,你选择的制备C02反应的化学方程式为 .在工业生产中,要获得生产纯碱的原料CO2你认为最经济实用的方法是以 为原料,该反应的化学方程式为 .
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是 .
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是 .
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.) .在③中,将析出的晶体过滤后,溶液中数量减少的离子有 ;滤液中仍然存在的离子有 .②中反应的化学方程式为 .
(5)在20℃时,向含NH4HC0321g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4Cl. 查看习题详情和答案>>
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI.
材料2:四种盐在不同温度下的溶解度表.
| 温度 盐 溶解度 |
10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ------ | ------ |
| NaHCO3 | 8.1 | 9.6 | 11.1 | 12.7 | ---- |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(1)在实验室中,你选择的制备C02反应的化学方程式为
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.)
(5)在20℃时,向含NH4HC0321g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4Cl. 查看习题详情和答案>>
正确书写下列物质的化学式并列示计算相对分子质量.
氨气:
碳酸氢钠:
四氧化三铁:
碱式碳酸铜:
查看习题详情和答案>>
| 物质名称 | 化学式 | 相对分子质量 | 物质名称 | 化学式 | 相对分子质量 |
| 氨气 | NH3 NH3 |
17 17 |
碳酸氢钠 | NaHCO3 NaHCO3 |
84 84 |
| 四氧化三铁 | Fe3O4 Fe3O4 |
232 232 |
碱式碳酸铜 | Cu2(OH)2CO3 Cu2(OH)2CO3 |
222 222 |
14+1×3=17
14+1×3=17
;碳酸氢钠:
23+1+12+16×3=84
23+1+12+16×3=84
;四氧化三铁:
56×3+16×4=232
56×3+16×4=232
;碱式碳酸铜:
64×2+(16+1)×2+12+16×3=222
64×2+(16+1)×2+12+16×3=222
.