摘要:(3)CaC2+2H2O=C2H2↑+Ca(OH)2 C2H2 + CH3COOH CH3COOCH=CH2(4)①四周期.VIII族,3Fe2++NO3―+4H+= 3Fe3++NO↑+2H2O
网址:http://m.1010jiajiao.com/timu_id_318930[举报]
 A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:(1)若A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液,E溶于NaOH溶液的离子方程式是
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
;工业上冶炼A的化学反应方程式是2NaCl(熔融)
2Na+Cl2↑
| ||
2NaCl(熔融)
2Na+Cl2↑
.
| ||
(2)若C是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式是
CaC2+2H2O→C2H2↑+Ca(OH)2
CaC2+2H2O→C2H2↑+Ca(OH)2
;1mol C完全燃烧生成液态水时放热1300kJ,则C完全燃烧的热化学方程式是2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJ?mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJ?mol-1
.A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是Ca(HCO3)2
Ca(HCO3)2
.为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应.
请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式
(2)甲同学设计的实验
(a)使溴水褪色的反应,未必是加成反应
(b)使溴水褪色的反应,就是加成反应
(c)使溴水褪色的物质,未必是乙炔
(d)使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入括号,并写出装置内所放的化学药品.

(
(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是
查看习题详情和答案>>
请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式
CaC2+2H2O→C2H2↑+Ca(OH)2 HC≡CH+Br2→ 或HC≡CH+2Br2→
或HC≡CH+2Br2→
 或HC≡CH+2Br2→
或HC≡CH+2Br2→
CaC2+2H2O→C2H2↑+Ca(OH)2 HC≡CH+Br2→ 或HC≡CH+2Br2→
或HC≡CH+2Br2→
. 或HC≡CH+2Br2→
或HC≡CH+2Br2→
(2)甲同学设计的实验
不能
不能
(填能或不能)验证乙炔与溴发生加成反应,其理由是a、c
a、c
.(a)使溴水褪色的反应,未必是加成反应
(b)使溴水褪色的反应,就是加成反应
(c)使溴水褪色的物质,未必是乙炔
(d)使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是
H2S
H2S
,它与溴水反应的化学方程式是Br2+H2S═S↓+2HBr
Br2+H2S═S↓+2HBr
;在验证过程中必须全部除去.(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入括号,并写出装置内所放的化学药品.

(
c
c
)→(b)→(CuSO4
CuSO4
)→(d)(硫酸铜)d
d
(溴水)(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是
如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证.
如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证.
.X、Y、Z、W是周期表中原子序数依次增大的前20号元素.X、Y同周期,Y、Z同主族.Zn-与Wn+离子的电子层结构相同.由这四种元素形成的单质、化合物有如图转化关系.已知:常温下A为液体,B、C、E、G为气态化合物,且A、C、G均为直线型分子;D是由元素W、Y形成的常见化合物.
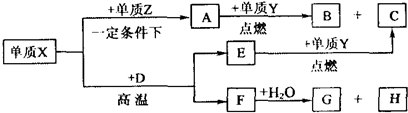
(1)元素W的名称
 ,A的电子式
,A的电子式
 .
.
(2)写出D、E的化学式:D:
(3)①已知38gA与Y完全反应生成B、C时放出akJ的热量,写出该反应的热化学方程式:
②F与水反应的化学方程式:
查看习题详情和答案>>

(1)元素W的名称
钙
钙
,Z的原子结构示意图



(2)写出D、E的化学式:D:
CaO
CaO
、E:CO
CO
.(3)①已知38gA与Y完全反应生成B、C时放出akJ的热量,写出该反应的热化学方程式:
CS2(l)+3O2(g)═CO2(g)+2SO2(g)△H=-2akJ/mol
CS2(l)+3O2(g)═CO2(g)+2SO2(g)△H=-2akJ/mol
.②F与水反应的化学方程式:
CaC2+2H2O→C2H2↑+Ca(OH)2
CaC2+2H2O→C2H2↑+Ca(OH)2
.甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等.已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子.
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
(3)在一定条件下,甲与O2反应的化学方程式是
(4)丁的元素符号是

(5)丁的氧化物的晶体结构与
查看习题详情和答案>>
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是
CaC2+2H2O═C2H2↑+Ca(OH)2
CaC2+2H2O═C2H2↑+Ca(OH)2
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
CO+CuO
CO2↑+Cu
| ||
CO+CuO
CO2↑+Cu
| ||
(3)在一定条件下,甲与O2反应的化学方程式是
N2+O2
2NO
| ||
N2+O2
2NO
| ||
(4)丁的元素符号是
Si
Si
,它的原子结构示意图为

(5)丁的氧化物的晶体结构与
金刚石
金刚石
的晶体结构相似.电石中的碳化钙和水能完全反应:
CaC2+2H2O=C2H2↑+Ca(OH)2
使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量.
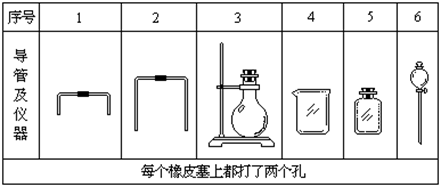
(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是 接 接 接 接 接 .
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞.
②检查装置的气密性.
③在仪器6和5中注入适量水.
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计).
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞.
正确的操作顺序(用操作编号填写)是 .
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有 杂质.
(4)若实验时称取的电石1.60克,测量排出水的体积后,折算成标准状况乙炔的体积为448毫升,此电石中碳化钙的百分含量是 %.
查看习题详情和答案>>
CaC2+2H2O=C2H2↑+Ca(OH)2
使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量.

(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞.
②检查装置的气密性.
③在仪器6和5中注入适量水.
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计).
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞.
正确的操作顺序(用操作编号填写)是
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有
(4)若实验时称取的电石1.60克,测量排出水的体积后,折算成标准状况乙炔的体积为448毫升,此电石中碳化钙的百分含量是