摘要:2.同主族元素 ①最外层电子数相同→化学性质相似. ②电子层数递增.半径递增→化学性质递变. ③非金属性渐弱.金属性渐强. ④最高价氧化物的水化物的酸性减弱.碱性增强.例如: eq \o(\s\up 2(H2CO3.H4SiO4.H4------------------------------ ⑤气态氢化物的稳定性减弱.还原性增强.例如: eq \o(\s\up 2(HF. HCl. HB-----------------------→
网址:http://m.1010jiajiao.com/timu_id_3186839[举报]
同一主族中,各元素原子最外层________相同,元素原子从上到下随着核电荷数的依次增加,电子层数依次________,失电子的能力________,得电子的能力________,因此元素的金属性依次________,非金属性依次________
查看习题详情和答案>>同一主族中,各元素原子最外层________相同,元素原子从上到下随着核电荷数的依次增大,电子层数________,原子半径________,失电子的能力________,得电子的能力________.元素的金属性________,非金属性________.
同一主族中,各元素原子最外层________相同,元素原子从上到下随着核电荷数的依次增加,电子层数依次________,失电子的能力________,得电子的能力________,因此元素的金属性依次________,非金属性依次________
查看习题详情和答案>>下列有关原子结构及元素周期律的叙述正确的是
| A.同主族元素的原子最外层电子数相同,化学性质也相同 |
| B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
(2012?岳阳二模)现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)已知BA5为离子化合物,写出其电子式
 .
.
(2)B基态原子中能量最高的电子,其电子云在空间有
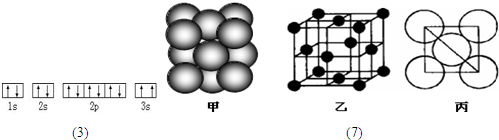
(3)某同学根据上述信息,推断C基态原子的核外电子排布如图:该同学所画的电子排布图违背了
(4)G位于
(5)DE3中心原子的杂化方式为
(6)检验F元素的方法是
(7)若某单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为
查看习题详情和答案>>
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |

(1)已知BA5为离子化合物,写出其电子式


(2)B基态原子中能量最高的电子,其电子云在空间有
3
3
个方向,原子轨道呈纺锤形
纺锤形
形(3)某同学根据上述信息,推断C基态原子的核外电子排布如图:该同学所画的电子排布图违背了
泡利原理
泡利原理
.(4)G位于
第ⅦB
第ⅦB
族d
d
区,价电子排布式为3d54s2
3d54s2
.(5)DE3中心原子的杂化方式为
sp3
sp3
,用价层电子对互斥理论推测其空间构型为三角锥形
三角锥形
.(6)检验F元素的方法是
焰色反应
焰色反应
,请用原子结构的知识解释产生此现象的原因是当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将以光的形式释放能量
当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将以光的形式释放能量
.(7)若某单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为
12
12
,该单质晶体中原子的堆积方式为四种基本模式中的铜型
铜型
.