摘要:非金属元素R的最高价含氧酸的组成为HnROn+2.该酸的分子量是M.R的原子量是 .该酸中R的化合价是 .在R的气态氢化物中R的化合价是 .该氢化物的组成可表示为 .
网址:http://m.1010jiajiao.com/timu_id_3184319[举报]
非金属元素R的最高价含氧酸的组成为HnROn+2,该酸的分子量是M,R的原子量是______,该酸中R的化合价是______,在R的气态氢化物中R的化合价是______,该氢化物的组成可表示为______。
查看习题详情和答案>>(6分)非金属元素R的最高价含氧酸的组成为HnROn+2,该酸的分子量是M,R的原子量是______,该酸中R的化合价是______,在R的气态氢化物中R的化合价是______,该氢化物的组成可表示为______。
查看习题详情和答案>>非金属元素R的最高价含氧酸的组成为HnROn+2,该酸的分子量是M,R的原子量是________,该酸中R的化合价是________,在R的气态氢化物中R的化合价是________,该氢化物的组成可表示为________。
查看习题详情和答案>>下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素.请用所给元素回答下列问题.
(1)某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为 ;与Ar原子具有相同电子层结构的简单离子中半径由大到小的顺序是(用离子符号表示) .
(2)M、D两种元素形成的化合物含有的化学键类型是 ,分子的电子式为: ;
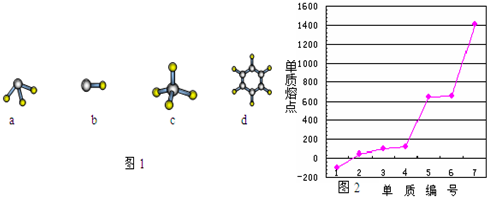
A与D形成分子的空间结构可能是如图1的(填序号) .
(3)保存T元素的二价硫酸盐需采取的措施是和理由是 ;所给元素中组成合适的反应物,用离子方程式表明元素M、R的非金属性强弱 .
(4)第三周期主族元素(零族除外)单质熔点高低的顺序如图2所示,“1”所代表物质的化学式是 ,“7”所对应的元素形成最高价氧化物的化学式是 .
查看习题详情和答案>>
| A | |||||||||||||||||
| D | E | ||||||||||||||||
| G | Q | M | R | ||||||||||||||
| T | |||||||||||||||||
(2)M、D两种元素形成的化合物含有的化学键类型是
A与D形成分子的空间结构可能是如图1的(填序号)

(3)保存T元素的二价硫酸盐需采取的措施是和理由是
(4)第三周期主族元素(零族除外)单质熔点高低的顺序如图2所示,“1”所代表物质的化学式是
(2010?柳州三模)A、B、C、D是常见不同主族的短周期元素,它们的原子序数逐渐增大,其中只有一种是金属元素,C元素原子最外层电子数是D元素原子最外层电子数的一半,B元素原子的最外层电子数比D的最外层电子数少两个.E、F也是短周期元素,E与D同主族,F与A同主族.
(1)写出F2E2的电子式
 .其中化学键类型为
.其中化学键类型为
(2)A、E、F 三种元素可形成一种离子化合物 R,用惰性电极电解 R 的稀溶液的化学反应方程式为
(3)六种元素中的三种组成的易溶于水的酸性物质中,能促进水电离的物质M是
(4)甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同.回答问题:
①向乙溶液中缓慢滴加过量的丙溶液过程中发生反应的离子方程式
②向甲溶液中缓慢滴加过量的丙溶液,所观察到的实验现象为
查看习题详情和答案>>
(1)写出F2E2的电子式


离子键和非极性共价键
离子键和非极性共价键
.(2)A、E、F 三种元素可形成一种离子化合物 R,用惰性电极电解 R 的稀溶液的化学反应方程式为
2H2O
2H2↑+O2↑
| ||
2H2O
2H2↑+O2↑
;电解一段时间后,溶液 pH
| ||
增大
增大
(填“增大”、“减小”或“不变”).(3)六种元素中的三种组成的易溶于水的酸性物质中,能促进水电离的物质M是
Al2(SO4)3等
Al2(SO4)3等
(写化学式,写一个即可,下同),能抑制水电离的物质N是H2SO4等
H2SO4等
.25℃时,pH=a的M溶液中水电离出的H+浓度与pH=a的N溶液中水电离出的H+浓度之比为1014-2a
1014-2a
.(4)甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同.回答问题:
①向乙溶液中缓慢滴加过量的丙溶液过程中发生反应的离子方程式
AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O
AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O
②向甲溶液中缓慢滴加过量的丙溶液,所观察到的实验现象为
先无明显现象,后产生大量无色气泡
先无明显现象,后产生大量无色气泡
.