网址:http://m.1010jiajiao.com/timu_id_309600[举报]
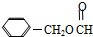 )是一种重要的工业使用的有机溶剂.分析如图的框图关系,然后回答问题:
)是一种重要的工业使用的有机溶剂.分析如图的框图关系,然后回答问题: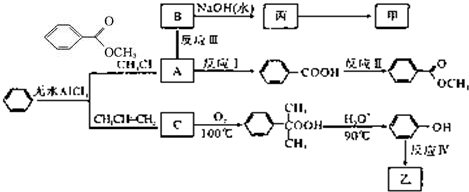
已知以下信息:
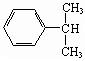
①有机化合物甲的结构:
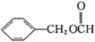
②有机化合物乙的结构:
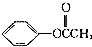
③有机化合物丙的分子式为C7H8O,熔融状态的丙能与钠反应放出氢气,且能够与乙酸发生酯化反应;
④苯在无水AlCl3的作用下与卤代烃、烯烃发生反应,可以在苯环上增加烷基.
(1)乙中含氧官能团的名称
(2)甲、乙、丙三种有机物中与苯甲酸甲酯是同分异构体的是
(3)写出C的结构简式:

(4)丙生成甲的反应类型与
a.反应I b.反应Ⅱc.反应Ⅲd.反应Ⅳ
(5)写出B生成丙的化学方程式:
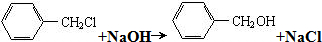
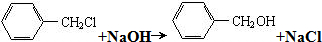
| 元素 | Mn | Fe | |
| 电离能( kJ?mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
回答下列问题:
(1)Mn元素价电子的电子排布式为
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氯和亚铁离子〔Fe(CN)64-〕中的配体CN-中C原子的杂化轨道类型是
(3)三氯化铁常温下为固体,熔点:282℃,沸点315℃,在300℃以上升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁的晶体类型为:
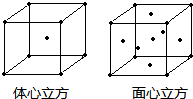
(4)金属铁的晶体在不同的温度下有两种堆积方式,晶体分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为:
(8分)已知由短周期元素组成的A、B、C、D四种常见化合物分子中所含原子数目依次为2、3、4、5,其中A、B含有18个电子,C、D含有10个电子。请回答:
(1)D中含有的化学键类型有 ,已知8gD与O2完全燃烧,生成稳定化合物时放出445kJ的热量,写出反应的热化学方程式 。
(2)室温下,若向一定量C的稀溶液中逐滴加入物质的量浓度相同的A,直至A过量,生成化合物XY4Z(X、Y、Z表示元素符号)。讨论上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH。试填写表中空白(要求填写有关粒子化学式):
|
|
离子浓度由大到小的顺序 |
溶质的化学式 |
溶液的pH |
|
I |
c(XY+4)>c(Z—)>c(OH—)>c(H+) |
|
pH>7 |
|
II |
c(XY+4)=c(Z—) |
XY4Z、XY3·H2O |
|
|
III |
|
XY4Z |
pH<7 |
|
IV |
c(Z—)>c(H+)>c(XY+4)> >c(OH—) |
|
pH<7 |
(3)B在空气中完全燃烧生成E,在一定条件下发生E与O2反应生成F。
①将0.05molE和0.03molO2放入容积为1L的密闭容器中,达到平衡,测得c(F)=0.04mol·L—1。计算该条件下反应的平衡常数K= 和E的平衡转化率 。
②已知上述反应是放热反应,当该反应处于平衡状态时,下列措施中有利于提高E平衡转化率的有 (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
查看习题详情和答案>>
氮元素可以形成多种分子和离子,如NH3、N2H4、N3-、NH4+、N2H62+等。回答以下问题:
(1)N的基态原子中,有 个运动状态不同的未成对电子。
(2)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布式是_______。
(3)NH3、N2H4、NH4+、N2H62+四种微粒中,同种微粒间能形成氢键的有____________;不能作为配位体的有____________。
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因 是 。
(5)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。
①N2H4分子中氮原子的杂化类型是______。
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)
若该反应中有4 mol N—H键断裂,则形成的π键有________mol。
(6)肼能与硫酸反应生成N2H6SO4。N2H6SO4化合物类型与硫酸铵相同,则N2H6SO4 内微粒间作用力不存在_______(填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
查看习题详情和答案>>