摘要:(4)Cl2+H2O H++Cl―+HClO,饱和食盐水Cl―浓度大.使上述平衡逆向移动.降低了Cl2在水中的溶解度
网址:http://m.1010jiajiao.com/timu_id_309587[举报]
(2013?通州区二模)四种短周期元素A、B、C、D的性质或结构信息如下:
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)B元素在周期表中的位置
(2)BC2分子的电子式
 ;
;
(3)A元素的单质与物质甲发生反应的离子方程式
(4)丙的钠盐溶液呈
(5)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液.滴加过程中的现象是:
①浅绿色溶液变成深棕黄色;
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间;
③试管底部出现红褐色沉淀.向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色.
请用化学方程式或离子方程式及必要的文字解释①、②、③中加点的字.
①
②
③
查看习题详情和答案>>
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)B元素在周期表中的位置
第2周期ⅣA族
第2周期ⅣA族
;(2)BC2分子的电子式


(3)A元素的单质与物质甲发生反应的离子方程式
Cl2+H2O?H++Cl-+HClO
Cl2+H2O?H++Cl-+HClO
;(4)丙的钠盐溶液呈
碱
碱
性,用化学用语表示其原因Cl-+H2O?HClO+OH-
Cl-+H2O?HClO+OH-
;(5)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液.滴加过程中的现象是:
①浅绿色溶液变成深棕黄色;
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间;
③试管底部出现红褐色沉淀.向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色.
请用化学方程式或离子方程式及必要的文字解释①、②、③中加点的字.
①
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
浅绿色Fe2+被过氧化氢氧化成黄色Fe3+(浓度大时呈深棕黄色)
浅绿色Fe2+被过氧化氢氧化成黄色Fe3+(浓度大时呈深棕黄色)
;②
2H2O2=2H2O+O2↑
2H2O2=2H2O+O2↑
;过氧化氢分解可产生氧气,常温时反应2H2O2=2H2O+O2↑较慢,因而开始气泡少;受热并且被逐渐增多的Fe3+催化,使反应速率加快而剧烈
过氧化氢分解可产生氧气,常温时反应2H2O2=2H2O+O2↑较慢,因而开始气泡少;受热并且被逐渐增多的Fe3+催化,使反应速率加快而剧烈
;③
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
.反应①使c(H+)降低且反应②放热,从而使水解平衡Fe3++3H2O?Fe(OH)3+3H+,正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀(因反应放热会使氢氧化铁部分分解为红棕色氧化铁)
反应①使c(H+)降低且反应②放热,从而使水解平衡Fe3++3H2O?Fe(OH)3+3H+,正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀(因反应放热会使氢氧化铁部分分解为红棕色氧化铁)
.(2000?上海)我国规定饮用水质量标准必须符合下列要求:
以下是源水处理成自来水的工艺流程示意图

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式
(2)凝聚剂除去悬浮固体颗粒的过程
①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4?7H2O常用的凝聚剂,它在水中最终生成
(3)通入二氧化碳的目的是
(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有
(5)下列物质中能作为氯气的代用品的是
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
查看习题详情和答案>>
| pH值 | 6.5-8.5 |
| Ca2+,Mg2+总浓度 | <0.0045mol/L |
| 细菌总数 | <100个/mL |

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式
HCO3-+OH-=CO32-+H2O;
HCO3-+OH-=CO32-+H2O;
(2)凝聚剂除去悬浮固体颗粒的过程
③
③
(填写编号,多选倒扣)①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4?7H2O常用的凝聚剂,它在水中最终生成
胶状Fe(OH)3
胶状Fe(OH)3
沉淀.(3)通入二氧化碳的目的是
除去Ca2+
除去Ca2+
和调节PH值
调节PH值
.(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有
强氧化
强氧化
性,请写出氯气与水反应的离子反应方程式Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
.(5)下列物质中能作为氯气的代用品的是
①③
①③
(填写编号,多选倒扣)①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
某同学应用如下所示装置研究物质的性质.其中气体C的主要成分是氯气,还含有少量空气和水蒸气.请回答下列问题: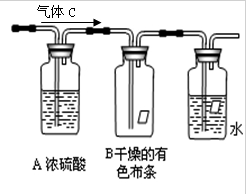
(1)该项研究的主要目的是
(2)浓硫酸的作用是
(3)观察到的实验现象是
(4)从物质性质角度来看,下图装置的实验设计还存安全隐患,表现在
查看习题详情和答案>>

(1)该项研究的主要目的是
探究氯气具有漂白性的条件
探究氯气具有漂白性的条件
.(2)浓硫酸的作用是
吸收气体C中的水
吸收气体C中的水
.(3)观察到的实验现象是
干燥布条不褪色,湿润的布条褪色
干燥布条不褪色,湿润的布条褪色
,有关反应的离子方程式Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
.(4)从物质性质角度来看,下图装置的实验设计还存安全隐患,表现在
没有尾气处理装置,造成环境污染
没有尾气处理装置,造成环境污染
,消除安全隐患的反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加2滴浓盐酸后,立即用另一培养皿扣在上面.

已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是:
(1)a处变
(2)c处的现象为
(3)e处变
(4)近年来科学家提出,高铁酸钾(K2FeO4)也可用作水处理剂.可用FeCl3与KClO在强碱性条件下反应制取,其反应的离子方程式为(不需要配平)
查看习题详情和答案>>

已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是:
(1)a处变
蓝
蓝
色,b处变橙
橙
色;(2)c处的现象为
试纸先变红,后褪色
试纸先变红,后褪色
,请说明原因Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色
Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色
;(3)e处变
红
红
色,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
、Fe3++3SCN-=Fe(SCN)3
Fe3++3SCN-=Fe(SCN)3
;(4)近年来科学家提出,高铁酸钾(K2FeO4)也可用作水处理剂.可用FeCl3与KClO在强碱性条件下反应制取,其反应的离子方程式为(不需要配平)
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
.下列为元素周期表中的一部分,按要求回答下列问题.
(1)这些元素中最不活泼的元素名称为:
(2)元素⑥⑦=10 ⑩的最高价氧化物对应的水化物中碱性最强的是:
(3)元素⑨的单质与H2O反应的离子方程式为:
(4)元素③的单质电子式为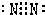
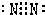 ;
;
(5)元素①③⑨形成的化合物中的化学键类型为:
(6)比较元素⑥⑦⑧⑨离子的半径由大到小的顺序为:
查看习题详情和答案>>
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
| 4 | =10 ⑩ | |||||||
氖
氖
;(2)元素⑥⑦=10 ⑩的最高价氧化物对应的水化物中碱性最强的是:
KOH
KOH
;(3)元素⑨的单质与H2O反应的离子方程式为:
Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
;(4)元素③的单质电子式为
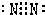
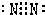
(5)元素①③⑨形成的化合物中的化学键类型为:
离子键和共价键
离子键和共价键
.(6)比较元素⑥⑦⑧⑨离子的半径由大到小的顺序为:
S2->Cl->Na+>Mg2+
S2->Cl->Na+>Mg2+
.