摘要:1.A:NH4NO3 C:Mg3N2 E:NH3
网址:http://m.1010jiajiao.com/timu_id_307516[举报]
如表是元素周期表的一部分.表中所列的字母分别代表某一化学元素,与实际元素符号无关.
(1)下列说法正确的是 .
A.第一电离能:A>B>E>J>K B.电负性:B>C>D>E>J
C.原子半径:F>G>H>E D.D、I分别与L形成的简单分子均为非极性分子
(2)表中A与E可形成A2E=E=EA2分子,有关该分子的说法不正确的是 .
A.分子中有6个σ键和2个π键
B.三个E原子都是sp2杂化
C.四个A原子不在同一平面内
D.三个E原子在同一条直线上
(3)F晶体的晶胞结构如图, 它的空间利用率为 (填“52%”、“68%”或“74%”).
它的空间利用率为 (填“52%”、“68%”或“74%”).
(4)字母K表示的元素原子基态时的价层电子排布式为 .
(5)MAL2晶体中包含的微粒间作用力有(填序号) .
①离子键 ②极性键 ③分子间作用力 ④金属键
(6)BHA4是一种络合物,中心原子配位数为 ,根据价层电子互斥理论可确定该物质中阴离子空间构型为 .
查看习题详情和答案>>
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | A | ||||||
| 2 | B | C | D | E | J | K | L |
| 3 | F | G | H | I | |||
| M |
A.第一电离能:A>B>E>J>K B.电负性:B>C>D>E>J
C.原子半径:F>G>H>E D.D、I分别与L形成的简单分子均为非极性分子
(2)表中A与E可形成A2E=E=EA2分子,有关该分子的说法不正确的是
A.分子中有6个σ键和2个π键
B.三个E原子都是sp2杂化
C.四个A原子不在同一平面内
D.三个E原子在同一条直线上
(3)F晶体的晶胞结构如图,
 它的空间利用率为
它的空间利用率为(4)字母K表示的元素原子基态时的价层电子排布式为
(5)MAL2晶体中包含的微粒间作用力有(填序号)
①离子键 ②极性键 ③分子间作用力 ④金属键
(6)BHA4是一种络合物,中心原子配位数为
(2010?天河区一模)下表为元素周期表的一部分,请参照元素A-H在表中的位置,用化学用语回答下列问题:
(1)上述元素中非金属性最强的元素是
(2)B、C、H的最高价含氧酸的酸性由强到弱的顺序是
(3)上述一元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(4)上述某元素的单质在常温下为气态,该元素能与A-H中一种元素构成原子个数比为1:1和1:2的两种共价化合物X、Y,还能与A-H中另一种元素构成原子个数比为1:1和1:2的两种离子化合物化合物Z、M,回答下列问题:
①写出物质X的电子式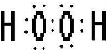
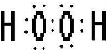 ;
;
②写出Z与Y反应的化学方程式
查看习题详情和答案>>
| 族 周期 |
IA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | B | C | D | E | ||||
| 3 | F | G | H | |||||
F
F
,金属性最强的是Na
Na
.(2)B、C、H的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3>H2SiO3
HNO3>H2CO3>H2SiO3
.D、E、F的原子半径由大到小的顺序为Na>O>F
Na>O>F
.(3)上述一元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
;(4)上述某元素的单质在常温下为气态,该元素能与A-H中一种元素构成原子个数比为1:1和1:2的两种共价化合物X、Y,还能与A-H中另一种元素构成原子个数比为1:1和1:2的两种离子化合物化合物Z、M,回答下列问题:
①写出物质X的电子式
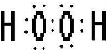
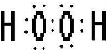
②写出Z与Y反应的化学方程式
2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2H2O═4NaOH+O2↑
.在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)该反应的化学方程式为
(2)20s时,N2O4的浓度为
(3)该反应的平衡常数表达式K=
,在80℃时该反应的平衡常数K值为
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
查看习题详情和答案>>
| 时间(s) C(mol/L) |
0 |
20 |
40 |
60 |
80 |
100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
N2O4?2NO2
N2O4?2NO2
,表中b>
>
c(填“<”、“=”、“>”).(2)20s时,N2O4的浓度为
0.14
0.14
mol/L,0~20s内N2O4的平均反应速率为0.003mol/L?s
0.003mol/L?s
.(3)该反应的平衡常数表达式K=
| c2(NO2) |
| c(N2O4) |
| c2(NO2) |
| c(N2O4) |
0.54
0.54
(保留2位小数).(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
ABD
ABD
.A、N2O4的转化率越高 B、NO2的产量越大C、N2O4与NO2的浓度之比越大 D、正反应进行的程度越大.I.在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)表中b
(2)80℃时,该反应的平衡常数K=
(3)在其他条件相同时,该反应的K值越大,表明建立平衡时
A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2有浓度之比越大D.正反应进行的程度越大
(4)要增大该反应的K值,可采取的措施
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂D.升高温度
(5)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.
查看习题详情和答案>>
| 时间/s c/mol?L-1 |
0 | 20 | 40 | 60 | 80 | 100 |
| N2O4 | 0.20 | a | 0.10 | c | d | e |
| NO2 | 0 | 0.12 | b | 0.26 | 0.30 | 0.30 |
(1)表中b
>
>
c(填“<”、“=”、“>”).0~20s内N2O4的平均反应速率为0.003mol/(L?s)
0.003mol/(L?s)
.(2)80℃时,该反应的平衡常数K=
1.8
1.8
.(3)在其他条件相同时,该反应的K值越大,表明建立平衡时
A、B、D
A、B、D
.A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2有浓度之比越大D.正反应进行的程度越大
(4)要增大该反应的K值,可采取的措施
D
D
.
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂D.升高温度
(5)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.
(2012?山东模拟)已知A、B、C、D、E是化学中常见的物质,其中E是一种无色无味的液体,它们之间有如下反应关系.
(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.
查看习题详情和答案>>

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.以下试剂中可用来区别C、D两种气体的是
| ||
①②④
①②④
.①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
当生成1molC时转移电子数是
| ||
2NA
2NA
.(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是
CaCl2、Ca(ClO)2
CaCl2、Ca(ClO)2
.(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是
②③
②③
.①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.