网址:http://m.1010jiajiao.com/timu_id_305275[举报]
一、 选择题(本题包括15小题,每小题只有一个选项符合题意,每题4分,共60分)
1 D 2. D 3. B 4. C 5. D 6. D 7.B 8. D 9. C
10 .B
二、选择题
16 AD 17 D 18D
【必做部分】
23.(12分)(1)图正确得2分
(2)电压U与电阻R的比值(或电流I)(2分):表格中各电流值分别为0.05,0.09,0.14,0.20,0.24,0.27(2分);图像如图所示(2分)
(3)2.00(1.98―2.02)(2分),0.45(0.40―0.50) (2分)

24.(15分)解:(1)运动员从最高点下落过程为平抛运动,竖直分运动为自由落体运动。设运动员起跳后重心离地的高度为H,则
 (2分)
(2分)
即 (2分)
(2分)
(2)设运动员脚刚触地时的竖直分速度为 。则由机械能守恒,
。则由机械能守恒,
 (4分)
(4分)
设运动员落地时受到的竖直方向的平均作用力为F,由动能定理得

 (4分)
(4分)
联立两式得 (3分)
(3分)
25.(18分)解:(1)粒子在第一象限做类平抛运动,
加速度 (3分)
(3分)
运动时间  (2分)
(2分)
沿 方向的位移
方向的位移
(2)粒子通过 轴进入磁场时在
轴进入磁场时在 方向上的速度
方向上的速度
 (2分)
(2分)
因此
粒子在第二象限以 为圆心做匀速圆周运动,圆弧所对的圆心角为
为圆心做匀速圆周运动,圆弧所对的圆心角为 ,运动时间
,运动时间

(3)粒子从磁场返回电场后的运动是此前由电场进入磁场运动的逆运动,经时间
粒子的速度变为 ,此后重复前面的运动。(2分)
,此后重复前面的运动。(2分)
粒子在电磁场中运动的周期 (2分)
(2分)
26. (15分)
(1)尝 X 甲病男女患者人数基本相同,乙病男性患者多余女性患者(2分) 基因突变(2)①aaXbY aaXBXb 或aaXBXb (不全不给分)
② 1/2 ③ 1/2 1/16 女
(3)增加 表兄妹之间有一部分基因相同(携带同种隐性致病基因的可能性较大)
(4)遗传咨询,产前诊断(2分)
27(18分)(1)神经-体液、免疫(2分) 含量少、作用大(2分)
(2)I 胰岛素(1分) 血糖利用、转化为糖元(2分) 非糖物质转化为血糖(肝糖元的分解)(2分)
II 反馈调节(2分)
III 细胞膜上受体蛋白不正常(或a激素不能与受体结合或控制 细胞膜上受体蛋白的基因发生突变所致)其他合理答案亦给分。(3分)
 (3)见下图,每图2分,共4分
(3)见下图,每图2分,共4分
28.(16分)
(1)Cu2S(2分) (2)Cu2S(2分)15mol(2分)
(3)酸雨中主要成分为H2SO3 :SO2-H2O=2H2SO2 (1分) H2SO3在空气中被氧化:
2H2SO3+O2=2H2SO4 (1分) 硫酸的酸性比亚硫酸强(1分)
(4)CuCO3?Cu(OH)2+4H-=2Cu2++3 H2O+CO2 (2分)
(5)否 (1分) Cu+2Fe3+= Cu2++2 Fe2+ (2分) 氯水(或双氧水) (2分)
29. (14分)
(1)0.1 (3分) (2)a (3分)
(3)①反应① (2分) Fe(OH)3+5OH-+3e-=Fe +4H2O
(3分)
+4H2O
(3分)
②强氧化性能杀菌消毒,其还原产物Fe3-水解[Fe3-+3H2O=Fe(OH)3(胶体)+3H-生成Fe(OH)3胶体能吸附水中杂质沉降而净水(3分)
30. (12分)
I (1)②(2分) (2)B (2分) (3)正确(2分)
II 从甲、乙两同学试验可以看出;
① 加热碳酸氢钠溶液至 离子水解,使溶液碱性增强(3分)
离子水解,使溶液碱性增强(3分)
② 当加热碳酸氢铵溶液至
31.略
32.(共8分)
(1)1 (1分) 2 (1分) ,三角锥形(1分)
(2)低于(1分) Cl2晶体属于分子晶体,Si晶体属于原子晶体,原子晶体中原子之间以很强的共价键结合,而分子晶体中分子间以较弱的分子间作用力结合,因而原子晶体的熔点比分子晶体的熔点高(2分)
(3)1s22s22p63s23p64s13d5(2分)
33.(8分)

(3)氧化反应 (2分)
34. (8分) (1)
(3)胶片上的蛋白膜存在时间的长短(或其他理由答案) (4)固定化酶
(5)萃取法、蒸馏法、压榨法(只要答出2条,就得2分)
(6)平板划线法 稀释涂布平板法
35. (8分) (1)核移植技术、动物细胞培养(缺一不给分)
(2)基因文库中提取,PCR技术扩增,人工化学合成(至少答对2项才能得分)启动子、终止子、标记基因(缺一不给分) 显微注射法
(3)胰蛋白酶或胶原蛋白酶 减数第二次分裂中期
(4)桑 胚和囊胚 节约资源、降低成本等(酌情给分)
胚和囊胚 节约资源、降低成本等(酌情给分)
36. (8分)
(1)  (1分)
(1分)  (1分)
(1分)
(2)①活塞缓慢下移,理想气体温度不变,内能不变,体积减小,外界度气体做功,根据热力学第一定律知,气体放热。(2分)
②根据玻意耳定律: (2分)
(2分)
活塞移动后气体的体积为: (2分)
(2分)
37. (8分)
解:(1)传播速度  (2分)
(2分)
(2)波由波源传到J所需时间 (1分)
(1分)
波刚传到J点时,J向上运动,到负的最大位移需时 (1分)
(1分)
所以总时间为 (1分)
(1分)
(3)图3分

38. (8分)
(1) 2(1分) 质子(或 ) (1分) ;
) (1分) ; (2分)
(2分)
(2)设加速后航天器的速度大小为 ,由动量守恒定律有
,由动量守恒定律有
 (3分)
(3分)
 (1分)
(1分)
(16分)铜在自然界中存在于多种矿石中,如
| 矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 |
|
|
|
|
请回答以下问题:
(1)上表所列铜的化合物中,铜的质量分数最高的是______________(填化学式)。
(2)工业上以黄铜矿为原料,采取火法熔炼工艺生产铜。该过程中有如下反应:
![]() ,该反应的还原剂是____________;若在标准状况下放出气体56L,则转移电子的物质的量为_____________。
,该反应的还原剂是____________;若在标准状况下放出气体56L,则转移电子的物质的量为_____________。
(3)某同学采集酸雨样品并测其pH,发现在一段时间内其pH逐渐减小。请用必要的文字和化学方程式说明其原因______________________________________________
________________________________________________________。
(4)铜制品长期置于潮湿的环境中,表面会产生一层铜绿,其主要成分与孔雀石相同。
请写出采用化学方法除去铜器表面铜绿的有关反应的离子方程式:_____________
_______________________________________________。
(5)![]() 与
与![]() 都是红色粉末。
都是红色粉末。![]() 溶于稀
溶于稀![]() 会生成
会生成![]() 和
和![]() 。一同学为鉴定某
。一同学为鉴定某![]() 样品中是否混有多少量的
样品中是否混有多少量的![]() ,设计了如下实验:取少量粉末放入足量稀
,设计了如下实验:取少量粉末放入足量稀![]() 中,向所得溶液中滴加
中,向所得溶液中滴加![]() 试剂。该同学通过实验认为:若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含
试剂。该同学通过实验认为:若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含![]() 。你认为这种说法是否正确___________:简述你的理由(用离子方程式表示):______________,
。你认为这种说法是否正确___________:简述你的理由(用离子方程式表示):______________,
如果要得到准确的结论,还需加入的一种试剂是_________________。
查看习题详情和答案>> 铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.(1)铁元素在元素周期表中的位置是
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示.
①该电池的总反应化学方程式为
②电池中NaCl的作用是
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为
(4)氯化铝广泛用于有机合成和石油工业的催化剂.将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式
| ||
| ||
(5)三氧化二铁和氧化亚铜(Cu2O)都是红色粉末,常用作颜料.已知氧化亚铜溶于稀硫酸生成Cu和CuSO4.取少量Fe2O3和Cu2O组成的混合物放入足量稀硫酸中.
①此过程中发生的反应有(用离子方程式表示):
Fe2O3+6H+=2Fe3++3H2O;
②设计实验证明反应后所得溶液中铁元素可能存在形式
③若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu2O)
请回答实验中有关问题:
实验一:探究红色粉末的成分
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO.
②Cu能与Fe2(SO4)3溶液作用生成CuSO4和FeSO4.
[提出假设]假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN溶液.
(1)若假设1成立,则实验现象是
(2)若假设2成立,则实验现象是
(3)若固体粉末完全溶解,滴加KSCN溶液时溶液不变红色,则此时发生反应的离子方程式为
[实验结果]经实验分析,假设3是正确的.
实验二:测定Cu2O的质量分数
(4)取a g该固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为
| 9(b-a) |
| a |
| 9(b-a) |
| a |
实验三:利用该红色粉末制取较纯净的胆矾(CuSO3?5H2O)
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下表:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
该实验小组设计实验方案如下:
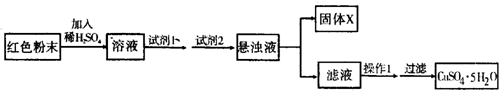
(5)请回答:
①试剂1为
②试剂2为
③固体X的化学式为
④操作I为
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式:
| ||
| ||
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | 加入H2O2 加入H2O2 |
把二价铁氧化成三价 把二价铁氧化成三价 |
| 步骤2 | 加入适量氧化铜,调节pH到3.7 加入适量氧化铜,调节pH到3.7 |
保证三价铁完全沉淀 保证三价铁完全沉淀 |
| 步骤3 | 过滤 过滤 |
滤出氢氧化铁 滤出氢氧化铁 |
| 步骤4 | 洗涤 | 除去杂质 除去杂质 |
| 步骤5 | 向沉淀中加入适量稀硫酸和适量铁粉 向沉淀中加入适量稀硫酸和适量铁粉 |
得到FeSO4溶液 |
| 144n |
| 64m |
查阅资料:Cu2O 溶于稀硫酸生成Cu和CuSO4;在空气中加热生成CuO.
提出假设:
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
(1)假设3:
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 溶液.
(2)若假设1成立,则实验现象是
(3)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?
(4)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是
探究延伸:经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(5)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为
| 9(b-a) |
| a |
| 9(b-a) |
| a |