摘要:
网址:http://m.1010jiajiao.com/timu_id_302085[举报]
一定条件下,可逆反应A2+B2?2AB达到化学平衡,经测定平衡时c(A2)=0.5mol?L-1,c(B2)=0.1mol?L-1,c(AB)=1.6mol?L-1,若A2、B2、AB的起始浓度分别以a、b、c表示.请回答:
(1)a、b应满足的关系是
(2)a的取值范围是
查看习题详情和答案>>
(1)a、b应满足的关系是
a-b=0.4
a-b=0.4
.(2)a的取值范围是
0.4<a<1.3
0.4<a<1.3
.在一容积固定的密闭容器中加入反应物A、B,发生如下反应:A+3B═2C.反应经2min后,A的浓度从开始时的1.20mol?L-1 下降到0.9mol?L-1,已知B的起始浓度为1.6mol?L-1.求:
(1)2min 末B、C的浓度:B
(2)2min 内该反应的平均速率:v(B)=
(3)反应物A的转化率为
查看习题详情和答案>>
(1)2min 末B、C的浓度:B
0.7
0.7
mol?L-1;C0.6
0.6
mol?L-1.(2)2min 内该反应的平均速率:v(B)=
0.45mol/(L.min)
0.45mol/(L.min)
; v(C)=0.3mol/(L.min)
0.3mol/(L.min)
.(3)反应物A的转化率为
25%
25%
.已知常温下甲醛是一种无色、有刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确认的致癌物和致畸物质之一.我国规定:居室中甲醛含量不得超过0.08mg/m3.可利用酸性高锰酸钾溶液测定甲醛含量.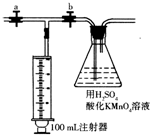
测定原理:KMnO4 (H+)溶液为强氧化剂,可氧化甲醛和草酸.
有关离子方程式为:4MnO4-+5HCHO+12H+→4Mn2++5CO2↑+11H2O;2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O;测定装置:部分装置如右图所示(a、b为止水夹).
测定步骤:
①收集待检新装修的房屋居室空气5L.
②准确量取5.00mL 1.00×10-3mol/L的高锰酸钾溶液于250mL锥形瓶中,滴入3滴6mol/L
的H2SO4溶液,加水45mL稀释,备用.
③将1.00×10-3mol/L的草酸标准溶液置于酸式滴定管中备用.
④打开a,关闭b,用注射器抽取100mL新装修的房屋的室内空气.关闭a,打开b,缓缓推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应.再如此重复4次.
⑤用标准草酸溶液滴定锥形瓶中的溶液,记录滴定所消耗的草酸溶液的体积.
⑥再重复实验2次(每次所取的高锰酸钾溶液均为5.00mL).3次实验所消耗草酸溶液的体积平均值为12.38mL.回答以下问题:
(1)使用
(2)如果注射器压送气体速度过快,可能会产生什么不良后果?使结果偏高还是偏低?
(3)本实验是否需要外加指示剂?若需要请指出指示剂的名称,若不需要,试说明如何确定滴定的终点.
(4)计算该居室内空气中甲醛的浓度
查看习题详情和答案>>

测定原理:KMnO4 (H+)溶液为强氧化剂,可氧化甲醛和草酸.
有关离子方程式为:4MnO4-+5HCHO+12H+→4Mn2++5CO2↑+11H2O;2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O;测定装置:部分装置如右图所示(a、b为止水夹).
测定步骤:
①收集待检新装修的房屋居室空气5L.
②准确量取5.00mL 1.00×10-3mol/L的高锰酸钾溶液于250mL锥形瓶中,滴入3滴6mol/L
的H2SO4溶液,加水45mL稀释,备用.
③将1.00×10-3mol/L的草酸标准溶液置于酸式滴定管中备用.
④打开a,关闭b,用注射器抽取100mL新装修的房屋的室内空气.关闭a,打开b,缓缓推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应.再如此重复4次.
⑤用标准草酸溶液滴定锥形瓶中的溶液,记录滴定所消耗的草酸溶液的体积.
⑥再重复实验2次(每次所取的高锰酸钾溶液均为5.00mL).3次实验所消耗草酸溶液的体积平均值为12.38mL.回答以下问题:
(1)使用
酸式滴定管
酸式滴定管
量取5.00mL高锰酸钾溶液.(2)如果注射器压送气体速度过快,可能会产生什么不良后果?使结果偏高还是偏低?
甲醛来不及被吸收,影响测定结果;使结果偏低
甲醛来不及被吸收,影响测定结果;使结果偏低
.(3)本实验是否需要外加指示剂?若需要请指出指示剂的名称,若不需要,试说明如何确定滴定的终点.
不需要,以高锰酸钾为指示剂,最后一滴草酸标准溶液滴下,溶液紫红色褪去且半分钟内不恢复,即为滴定终点
不需要,以高锰酸钾为指示剂,最后一滴草酸标准溶液滴下,溶液紫红色褪去且半分钟内不恢复,即为滴定终点
.(4)计算该居室内空气中甲醛的浓度
3.6
3.6
mg/m3,该居室的甲醛是
是
(填“是”或“否”)超标.Ⅰ某温度下,密闭容器中充入1mol N2和3mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为w,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为w,N2、H2、NH3的物质的量分别用x、y、z表示.
(1)恒温恒容条件下:若x=0.75mol,则y=
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是
Ⅱ一定条件下,可逆反应X(g)+Y(g) 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y)=0.1mol/L; c (Z)=1.6mol/L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y)=0.1mol/L; c (Z)=1.6mol/L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是
Ⅲ在10℃和4×105Pa的条件下,当反应aA(g) dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
(1)压强从4×105Pa增加到6×105Pa时,平衡向
(2)压强从10×105Pa增加到20×105Pa时,平衡向
查看习题详情和答案>>
(1)恒温恒容条件下:若x=0.75mol,则y=
2.25
2.25
,z=0.5
0.5
.(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是
x:y=1:3
x:y=1:3
.Ⅱ一定条件下,可逆反应X(g)+Y(g)
 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y)=0.1mol/L; c (Z)=1.6mol/L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y)=0.1mol/L; c (Z)=1.6mol/L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是a=b+0.4
a=b+0.4
,a的取值范围为0.4≤a≤1.3
0.4≤a≤1.3
Ⅲ在10℃和4×105Pa的条件下,当反应aA(g)
 dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
逆
逆
(填“正”或“逆”)方向移动,理由是压强从4×105Pa到6×105Pa时,增加为原来的1.5倍,而c(D)=6/4×0.085mol/L=0.128mol/L>0.126,所以实际平衡向逆反应方向移动
压强从4×105Pa到6×105Pa时,增加为原来的1.5倍,而c(D)=6/4×0.085mol/L=0.128mol/L>0.126,所以实际平衡向逆反应方向移动
(2)压强从10×105Pa增加到20×105Pa时,平衡向
正
正
(填“正”或“逆”)方向移动.