摘要:2Al2O3 4Al+3O2↑②Fe用高温还原剂法:
网址:http://m.1010jiajiao.com/timu_id_286205[举报]
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是
(2)ZW2常温下呈液态,形成晶体时,属于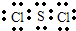
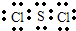 .
.
(3)工业生产单质Y的原理是
(4)X与Y化学性质相似,则等物质的量的X与Y与足量的浓NaOH溶液反应产生的H2的物质的量之比为
(5)0.1mol的单质W与50mL 1.5mol?L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是
查看习题详情和答案>>
(1)Y、Z、W的原子半径由小到大的顺序是
Cl<S<Al
Cl<S<Al
(用对应元素符号表示).(2)ZW2常温下呈液态,形成晶体时,属于
分子
分子
晶体,它的电子式是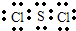
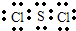
(3)工业生产单质Y的原理是
2Al2O3(熔融)
4Al+3O2↑
| ||
2Al2O3(熔融)
4Al+3O2↑
(用化学方程式表示).
| ||
(4)X与Y化学性质相似,则等物质的量的X与Y与足量的浓NaOH溶液反应产生的H2的物质的量之比为
2:3
2:3
.(5)0.1mol的单质W与50mL 1.5mol?L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是
3:5
3:5
.下列常见金属的冶炼原理中不合理的是( )
| 金属 | 冶炼原理 | |||||
| A | Fe | Fe2O3+3CO
| ||||
| B | Hg | 2HgO
| ||||
| C | Al | 2Al2O3
| ||||
| D | Na | 2NaCl(熔融)
|
| A、A | B、B | C、C | D、D |
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ?????????? ,下列可作阴极材料的是________________。
A.铝材 ????????? B.石墨 ????????? C.铅板 ?????????? D.纯铝

(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为__________________________________。
(4)在铝阳极氧化过程中,需要不断地调整电压,理由是____________?????????????? 。
(5)下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
查看习题详情和答案>>
(1)航天飞机曾用金属铝粉和高氯酸铵混合物作为固体燃料.加热铝粉使其氧化并放出大量热量,促使混合物中另一种燃料分解.m mol高氯酸铵分解时除产生2m mol水蒸气和m mol氧气外,其他组成元素均以单质形式放出,因而产生巨大的推动力.写出其中涉及到的化学方程式:
(2)高氯酸铵作为火箭燃料的重要氧载体.高氯酸铵在高压、450℃的条件下迅速分解生成水蒸气、氮气、氯化氢和氧气.
①写出此反应的化学方程式
②反应中生成的氧化产物与还原产物的物质的量之比是
查看习题详情和答案>>
4Al+3O2
2Al2O3、2NH4ClO4
N2↑+4H2O↑+Cl2↑+2O2↑
| ||
| ||
4Al+3O2
2Al2O3、2NH4ClO4
N2↑+4H2O↑+Cl2↑+2O2↑
;
| ||
| ||
(2)高氯酸铵作为火箭燃料的重要氧载体.高氯酸铵在高压、450℃的条件下迅速分解生成水蒸气、氮气、氯化氢和氧气.
①写出此反应的化学方程式
4NH4ClO4
6H2O↑+2N2↑+4HCl↑+5O2↑
| ||
| 450℃ |
4NH4ClO4
6H2O↑+2N2↑+4HCl↑+5O2↑
;
| ||
| 450℃ |
②反应中生成的氧化产物与还原产物的物质的量之比是
7:4
7:4
,每分解1mol高氯酸铵,转移的电子数目是8NA或8×6.02×1023
8NA或8×6.02×1023
.将洁净的金属片Fe、Zn、A、B分别与Cu用导线连接浸在合适的电解质溶液里.实验并记录电压指针的移动方向和电压表的读数如下表所示:
根据实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越
(2)Zn、A、B三种金属活动性由强到弱的顺序是
(3)Cu与A组成的原电池,
(4)A、B形成合金,露置在潮湿空气中,
(5)铝热反应中的铝热剂的成分是
查看习题详情和答案>>
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | -0.15 |
| B | B→Cu | +0.3 |
(1)构成两电极的金属活动性相差越大,电压表的读数越
大
大
.(填“大”、“小”).(2)Zn、A、B三种金属活动性由强到弱的顺序是
Zn>B>A
Zn>B>A
.(3)Cu与A组成的原电池,
Cu
Cu
为负极,此电极反应式为Cu-2e-=Cu2+
Cu-2e-=Cu2+
.(4)A、B形成合金,露置在潮湿空气中,
B
B
先被腐蚀.(5)铝热反应中的铝热剂的成分是
铝粉和金属氧化物的混合物
铝粉和金属氧化物的混合物
,工业上常用的铝的冶炼的化学方程式为2Al2O3
4Al+3O2↑
| ||
2Al2O3
4Al+3O2↑
.
| ||