摘要:4AgNO3+2H2O 4Ag↓+O2↑+4HNO3[提问]在溶液中能实现Mg2+→Mg,Al3+→Al和Na+.Na吗?为什么?学生:Na+.Mg2+.Al3+的得电子能力比溶液中的H+强.所以很难被还原成金属.[讲解]由此可以看出.随着不同金属的阳离子的氧化能力不同.主要有:电解法.还原剂法.加热法等.我们可以根据金属活动顺序把金属冶炼的方法规律总结如下:学生思考.记笔记: K.Ca.Na.Mg.Al.Zn.Fe.Sn.Pb(H)Cu.Hg.Ag.Pt.Au.熔融电解法 高温还原剂法 加热法 溶液电解法金属阳离子:得电子:弱→强[投影――内容见右][提问]请同学通过Na.Al.Fe.Hg的生成冶炼的方法.写出化学方程式.学生回答:①Na和Al用熔融电解法冶炼:
网址:http://m.1010jiajiao.com/timu_id_286203[举报]
A、B、C三种强电解质,它们溶于水在水中电离出的阳离子有K+、Ag+,阴离子有NO3-、OH-(电解质电离的离子有重复).
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极.接通电源,经过一段时间后,测得甲中b电极质量增加了43.2g.常温下各烧杯中溶液pH与电解时间t关系如图2.请回答下列问题: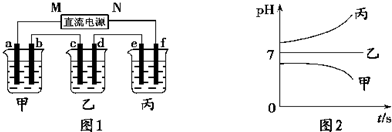
(1)写出三种强电解质的化学式:A
(2)写出乙烧杯c电极发生的电极反应为
(3)计算丙烧杯e电极上生成的气体在标准状况下的体积为
(4)要使甲烧杯中的A溶液恢复到电解前的状态,需要加入的物质是
(5)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液时H2SO4,则放电时N级上发生的电极反应为
查看习题详情和答案>>
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极.接通电源,经过一段时间后,测得甲中b电极质量增加了43.2g.常温下各烧杯中溶液pH与电解时间t关系如图2.请回答下列问题:

(1)写出三种强电解质的化学式:A
AgNO3
AgNO3
;BKNO3
KNO3
;CKOH
KOH
.(2)写出乙烧杯c电极发生的电极反应为
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
,甲烧杯中的总反应的化学方程式为4AgNO3
4Ag+O2↑+4HNO3
| ||
4AgNO3
4Ag+O2↑+4HNO3
.
| ||
(3)计算丙烧杯e电极上生成的气体在标准状况下的体积为
2.24L
2.24L
,甲烧杯中溶液体积为400ml,pH=0
0
.(4)要使甲烧杯中的A溶液恢复到电解前的状态,需要加入的物质是
Ag2O
Ag2O
,其质量为46.4g
46.4g
.(5)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液时H2SO4,则放电时N级上发生的电极反应为
Pb-2e-+SO42-=PbSO4
Pb-2e-+SO42-=PbSO4
,M级附近溶液的pH升高
升高
(选填“升高”或“降低”或“不变”).铅蓄电池充电时,若阳极和阴极之间用阳离子交换膜(只允许H+通过)隔开,则当外电路通过0.2mol电子时,由阳极室通过阳离子交换膜进入阴极室的阳离子有0.2
0.2
mol. 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是AgNO3溶液,电解之前在两极各滴入几滴石蕊试液,则
①Y电极上的电极反应式是
4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
,在Y极附近观察到的现象是
放出无色无味的气体,且溶液变红
放出无色无味的气体,且溶液变红
.②电解总反应离子方程式为
4Ag++2H2O═4Ag+O2↑+4H+
4Ag++2H2O═4Ag+O2↑+4H+
.(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是
纯铜
纯铜
,②Y电极的电极反应式是Cu-2e-=Cu2+
Cu-2e-=Cu2+
(说明:杂质发生的电极反应不必写出)
③假若电路中有0.04摩尔电子通过时,阴极增重
1.28
1.28
克.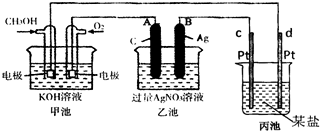 如图是一个化学过程的示意图.
如图是一个化学过程的示意图.(1)请回答图中甲池是
原电池
原电池
装置,其中OH-移向CH3OH
CH3OH
极(填“CH3OH”或“O2”)(2)写出通入CH3OH的电极的电极反应式是
CH3OH-6e-+8OH-=CO32-+6H2O
CH3OH-6e-+8OH-=CO32-+6H2O
.(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为
A
A
极(填“A”或“B”),并写出此电极反应的电极反应式4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
.(4)乙池中反应的离子方程式为
4Ag++2H2O=4Ag+O2↑+4H+
4Ag++2H2O=4Ag+O2↑+4H+
.(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是
1
1
(若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是BD
BD
(填序号)A.MgSO4 B.CuSO4 C.NaCl D.AgNO3.
 4Ag+O2↑+4H
4Ag+O2↑+4H