摘要:CO2 CO,
网址:http://m.1010jiajiao.com/timu_id_286195[举报]
 CO和H2与我们的生产和生活等方面密切相关.
CO和H2与我们的生产和生活等方面密切相关.(1)将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.
已知:C(s)+O2(g)=CO2(g)△H=-393.5kJ.mol-1
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
则C(s)与水蒸气反应制取CO和H2的热化学方程式为
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ.mol-1
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ.mol-1
.标准状况下,V( CO):V(H2)=1:l的水煤气22.4L,完全燃烧生成CO2和水蒸气,放出的热量为262.5kJ
262.5kJ
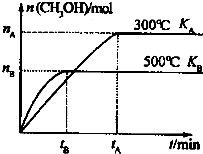
.(2)一定条件下,在容积为3L的密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),达平衡状态.根据图示回答:
①500℃时,从反应开始至达到平衡状态V(H2)=
| 2nB |
| 3tB |
| 2nB |
| 3tB |
②KA 和KB的关系是:KA
>
>
KB,该反应的△H<
<
0(填“>”、“=”或“<”).③300℃达平衡时,将容器容积压缩到原来的
| 1 |
| 2 |
>
>
v(逆)(填“大于”、“等于”或“小于”).(3)室内煤气泄漏造成人体中毒,是因为CO吸入肺中与输氧血红蛋白(HbO2)发生反应:CO+HbO2?O2+HbCO,37℃时,K=220.当[HbCO]:[HbO2]≥0.02时,即吸入CO与O2物质的量浓度之比≥
1:11000
1:11000
时,人的智力会受损;把CO中毒的病人放入高压氧舱中解毒的原理是氧气浓度增大,上述化学平衡逆向移动,使CO从血红蛋白中脱离出来
氧气浓度增大,上述化学平衡逆向移动,使CO从血红蛋白中脱离出来
. CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是
acd
acd
(填序号)a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟利昂排放
c.多步行或乘公交车,少用私家车
d.将工业废气用碱液吸收后再排放
(2)有学者设想以如图所示装置用电化学原理将CO2、SO2转化为重要化工原料.
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为
CO2+6H++6e-=CH3OH+H2O
CO2+6H++6e-=CH3OH+H2O
;②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为
SO2+2H2O-2e-=4H++SO42-
SO2+2H2O-2e-=4H++SO42-
;当电路中有1mole-流过,正极区溶液中的H+的物质的量的变化量△n(H+)=
1
1
mol.(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:17℃、1.01×l05Pa时,2NO2(g)?N2O4(g)△H<0的平衡常数K=13.3.
①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol?L-1,则c(N2O4)=
0.012mol/L
0.012mol/L
(保留两位有效数字)②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol?L-1,c(N2O4)=0.007mol?L-1,则改变的条件为
升温
升温
.(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料.
①由CO和H2合成甲醇的方法是CO(g)+2H2(g)?CH3OH(g),己知该反应在300°C时的化学平衡常数为0.27,该温度下将2mol CO、3mol H2利2molCH3OH(g)充入容积为2L的密闭容器中,此时反应将
向逆反应方向进行
向逆反应方向进行
(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”).②己知:
a.用合成气(CO和H2)生产甲醇(CH3OH),合成1mol CH3OH(l)吸收热量131.9kJ
b.2H2(g)+CO(g)+
| 3 |
| 2 |
CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-726KJ/mol
| 3 |
| 2 |
CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-726KJ/mol
.| 3 |
| 2 |
CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置.
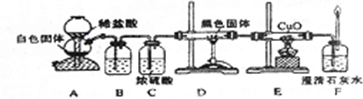
已知:C+H2O
CO+H2 C+H2O
CO2+H2 C+CO2
2CO
试回答下列问题:
①装置B中最适宜的试剂是
②根据该实验中的
③若要根据装置P中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置
查看习题详情和答案>>

已知:C+H2O
| ||
| ||
| ||
试回答下列问题:
①装置B中最适宜的试剂是
饱和碳酸氢钠溶液
饱和碳酸氢钠溶液
,必须用装置C吸收气体中的水蒸气的理由是防止水蒸气与炭反应生成的氢气对实验现象产生干扰
防止水蒸气与炭反应生成的氢气对实验现象产生干扰
;②根据该实验中的
E装置中黑色CuO变红色
E装置中黑色CuO变红色
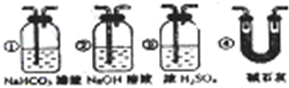
现象,可证明CO具有还原性;③若要根据装置P中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置
D
D
与E
E
之间(填字母标号)连接如图中的④
④
装置(选填序号).
CO、CH4均为常见的可燃性气体.
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为
②若燃烧后气体体积缩小了
mL,则a与b关系的数学表达式是
查看习题详情和答案>>
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
1:4
1:4
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是
CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H=-891.45kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H=-891.45kJ/mol
.(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为
0.33
0.33
(保留2位小数).②若燃烧后气体体积缩小了
| a |
| 4 |
b≥
a
| 5 |
| 4 |
b≥
a
.| 5 |
| 4 |
 CO(g)与H2O(g)反应过程的能量变化如图所示,有关两者反应说法正确的是( )
CO(g)与H2O(g)反应过程的能量变化如图所示,有关两者反应说法正确的是( )