摘要:思考讨论:</PGN0070.TXT/PGN>回答:在同一容器中投入2molPCl5可相当于容器的体积减小一半.相当于对第一个平衡体系增大压强.使平衡向左移动.PCl5的量增大.B正确.[引导]为了回避这样的问题.我们可以进行思维代换.把浓度的改变代换为体积的改变.然后再代换为压强的改变.[启示]当需要比较两个相同的可逆反应的不同平衡状态时.即可采用这样的代换思维方法:①转换为平衡移动问题,
网址:http://m.1010jiajiao.com/timu_id_285966[举报]
某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们好奇地对钠在CO2气体中燃烧进行了实验:
【实验过程】将玻璃燃烧匙中燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上黏附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,说明可燃物燃烧的条件:_________________。
(2)要使燃烧的钠熄灭,可选用的灭火剂是___________。
A.水 B.干沙子 C.二氧化碳 D.四氯化碳
【探究问题】燃烧后瓶壁上附着的白色物质是什么?
【提出假设】①白色物质是Na2O2 ②白色物质是Na2CO3 ③白色物质是Na2O和Na2CO3的混合物。
【实验验证】该小组对燃烧后的白色物质进行如下探究
【实验过程】将玻璃燃烧匙中燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上黏附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,说明可燃物燃烧的条件:_________________。
(2)要使燃烧的钠熄灭,可选用的灭火剂是___________。
A.水 B.干沙子 C.二氧化碳 D.四氯化碳
【探究问题】燃烧后瓶壁上附着的白色物质是什么?
【提出假设】①白色物质是Na2O2 ②白色物质是Na2CO3 ③白色物质是Na2O和Na2CO3的混合物。
【实验验证】该小组对燃烧后的白色物质进行如下探究

【思考讨论】
(3)①通过方案l和方案2的实验,你认为上述三个假设中,____成立。
②钠在二氧化碳中燃烧的化学方程式为______________________。
③丙同学认为白色物质有可能是氢氧化钠,否定他的观点的理由是_____________________。
【拓展思维】
(4)某碳酸钠粉末中可能含有少量的氢氧化钠和氯化钠,为检验该粉末中是否含有这些物质,某学生计划分六个步骤,其中四个步骤所用的试剂及实验操作已写明。请将下面表格里补写完整尚缺的②⑤两个步骤所用的试剂及实验操作。
(3)①通过方案l和方案2的实验,你认为上述三个假设中,____成立。
②钠在二氧化碳中燃烧的化学方程式为______________________。
③丙同学认为白色物质有可能是氢氧化钠,否定他的观点的理由是_____________________。
【拓展思维】
(4)某碳酸钠粉末中可能含有少量的氢氧化钠和氯化钠,为检验该粉末中是否含有这些物质,某学生计划分六个步骤,其中四个步骤所用的试剂及实验操作已写明。请将下面表格里补写完整尚缺的②⑤两个步骤所用的试剂及实验操作。

化学科研小组的同学在精确测试Na2SO3溶液的pH时,遇到了困惑.为此,他们进行了冷静的思考和准备,决心重新实验,揭开奥秘.请你了解情况,参与交流讨论.
[查阅资料]①常温下0.1mol?L-1的H2SO3溶液的pH约为2.1.
②通常情况下,H2S为无色,有腐蛋臭味的气体,其水溶液称为氢硫酸.常温下0.1mol?L-1的H2S溶液的pH约为4.5.
[实验操作]①准确称取纯净的Na2SO3?7H2O晶体25.20g,配成1L水溶液,测得其pH=7.8.
②以坩埚再次准确称取25.20g上述晶体,继而隔绝空气在600℃以上高温下强热至恒重,质量为12.60g.
③将②所得之12.60g固体进行元素定性定量分析,组成与Na2SO3无异.将其溶于水得250mL溶液,测得pH=10.3.
[分析猜想]Na2SO3?7H2O在强热下,失去结晶水,进而发生了分解反应(自身氧化还原反应)
[交流讨论]
(1)实验操作②中称量操作至少进行
(2)给Na2SO3?7H2O加热时要隔绝空气,请以简要的文字和化学方程式给以说明.
(3)猜想Na2SO3在高温强热下发生分解反应的化学方程式是
(4)实验①和③中,两次测得的溶液pH相差明显,其合理的解释是
(5)请你设计简单的实验方案,给上述分析、猜想及解释以佐证.请简单叙述实验步骤、现象和结论.
查看习题详情和答案>>
[查阅资料]①常温下0.1mol?L-1的H2SO3溶液的pH约为2.1.
②通常情况下,H2S为无色,有腐蛋臭味的气体,其水溶液称为氢硫酸.常温下0.1mol?L-1的H2S溶液的pH约为4.5.
[实验操作]①准确称取纯净的Na2SO3?7H2O晶体25.20g,配成1L水溶液,测得其pH=7.8.
②以坩埚再次准确称取25.20g上述晶体,继而隔绝空气在600℃以上高温下强热至恒重,质量为12.60g.
③将②所得之12.60g固体进行元素定性定量分析,组成与Na2SO3无异.将其溶于水得250mL溶液,测得pH=10.3.
[分析猜想]Na2SO3?7H2O在强热下,失去结晶水,进而发生了分解反应(自身氧化还原反应)
[交流讨论]
(1)实验操作②中称量操作至少进行
4
4
次.(2)给Na2SO3?7H2O加热时要隔绝空气,请以简要的文字和化学方程式给以说明.
避免Na2SO3被氧化,2Na2SO3+O2=2Na2SO4
避免Na2SO3被氧化,2Na2SO3+O2=2Na2SO4
.(3)猜想Na2SO3在高温强热下发生分解反应的化学方程式是
4Na2SO3
Na2S+3Na2SO4
| ||
4Na2SO3
Na2S+3Na2SO4
.
| ||
(4)实验①和③中,两次测得的溶液pH相差明显,其合理的解释是
实验③的溶液中可能有Na2S,相同条件下,S2-水解程度大于SO32-,溶液的碱性强
实验③的溶液中可能有Na2S,相同条件下,S2-水解程度大于SO32-,溶液的碱性强
.实验③中溶液的pH=10.3的原理是(以相关的离子方程式表示)S2-+H2O HS-+OH-
HS-+OH-
 HS-+OH-
HS-+OH-S2-+H2O HS-+OH-
HS-+OH-
. HS-+OH-
HS-+OH-(5)请你设计简单的实验方案,给上述分析、猜想及解释以佐证.请简单叙述实验步骤、现象和结论.
取③溶液适量于试管中,向其中加稀H2SO4,如有腐蛋气味气体生成,则证明有S2-
取③溶液适量于试管中,向其中加稀H2SO4,如有腐蛋气味气体生成,则证明有S2-
、另取③中溶液适量于试管中,加入HCl酸化的BaCl2,如有白色沉淀生成,证明有SO42-
另取③中溶液适量于试管中,加入HCl酸化的BaCl2,如有白色沉淀生成,证明有SO42-
. (2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:[实验一]:研究性学习小组甲以铜为电极电解饱和食盐水,探究过程如下:
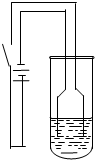
实验过程:按如图装置,接通电源后,阴极产生大量气泡;阳极铜丝由粗变细,不久出现砖红色浑浊,最后在试管底部聚集砖红色沉淀,溶液始终未出现蓝色.
查阅资料:某些铜的化合物有关性质如表所示:
| 物质 | 性质 | 物质 | 性质 |
| 氯化铜 | 浓溶液呈绿色,稀溶液呈蓝色 | 氯化亚铜 | 白色 |
| 氧化亚铜 | 砖红色,在酸性条件下易反应: Cu2O+2H+=Cu+Cu2++H2O. Cu2O在空气中灼烧生成CuO |
氢氧化亚铜 | 橙黄色,不稳定 |
(1)试管底部砖红色沉淀的化学式为
Cu2O
Cu2O
.(2)写出电解总反应方程式
2Cu+H2O
Cu2O+H2↑
| ||
2Cu+H2O
Cu2O+H2↑
.
| ||
[实验二]研究性学习小组乙为检测[实验一]生成的砖红色沉淀中是否含有Cu,设计了以下两种方案进行探究.
方案1:取少量砖红色沉淀溶于足量的浓硝酸中,观察溶液颜色变化.
方案2:取一定质量砖红色沉淀在空气中充分灼烧,根据灼烧前后质量变化进行判断.
(3)请你评价方案1和方案2是否合理,并简述其原因.
方案1
不合理,因为铜和氧化亚铜都能与硝酸生成Cu2+
不合理,因为铜和氧化亚铜都能与硝酸生成Cu2+
.方案2
合理,因为等质量的Cu2O与Cu2O、Cu的混合物在空气中灼烧前后质量变化不同
合理,因为等质量的Cu2O与Cu2O、Cu的混合物在空气中灼烧前后质量变化不同
.思考与交流:实验结束后,同学们关于[实验二]中“方案一”溶液呈绿色,而不呈蓝色展开了讨论.丙同学认为是该溶液中硝酸铜的质量分数较高所致;丁同学则认为是该溶液中溶解了生成的气体.
(4)同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中不可行的是(选填序号字母)
B
B
.A、加热该绿色溶液,观察颜色变化.
B、加水稀释绿色溶液,观察颜色变化
C、向该绿色溶液中通入氧气,观察颜色变化
D、向饱和的硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:[实验设计]
方法一:按照图1进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行.最终在
B
B
容器中观察到白色沉淀,该实验中涉及到的化学方程式有:Fe+H2SO4=FeSO4+H2↑、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、H2SO4+2NaOH=Na2SO4+2H2O
Fe+H2SO4=FeSO4+H2↑、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、H2SO4+2NaOH=Na2SO4+2H2O
.方法二:按图2进行实验,最终在两极间的溶液中首先观察到白色沉淀.请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水 ②NaCl溶液 ③NaOH溶液 ④四氯化碳 ⑤CuCl2溶液 ⑥乙醇 ⑦Fe棒 ⑧植物油 ⑨碳棒
a为
⑦
⑦
,b为⑨或⑦
⑨或⑦
,c为⑧
⑧
,d为②或③
②或③
.(填序号)[探究思考]实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3
由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3
;资料中提及的微绿色Fe3(OH)8,用氧化物的形式表示可写成FeO?Fe2O3?4H2O
FeO?Fe2O3?4H2O
.(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2?nH2O所致.用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势.
加热时,“方法一”中弹簧夹C应处于
打开
打开
(填“打开”或“关闭”)状态,容器A中的反应须处于发生
发生
(填“停止”或“发生”)状态.写出该实验中支持乙同学观点的化学方程式Fe(OH)2?nH2O
Fe(OH)2+nH2O
| ||
Fe(OH)2?nH2O
Fe(OH)2+nH2O
.
| ||
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路.
向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色
向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色
.某化学小组在讨论鉴别稀酸和浓硫酸的实验时,设计了如下表格.请按照给出的甲方案的式样,写出另外三种不同的鉴别方法.
(1)甲、乙两同学欲对上述整套装置检查气密性:
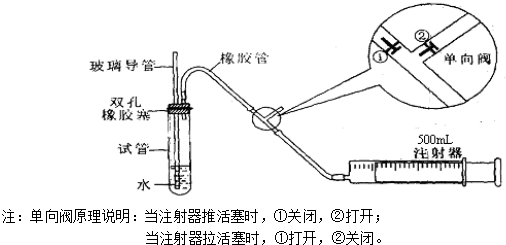
甲同学是用手捂住试管(或微热试管),观察导管中是否有液面上升的现象.是否能? (填能或不能);
乙同学是先从玻璃导管向试管中注入水,观察导管中液面与试管中液面是否形成高度差,且在一段时间后,观察液面差是否变化的方法.是否能? (填能或不能);
若上述两种方案均不能,请思考新方案,并填下列空白(若上述可行,则不填下列空白):先在试管中装入适量水(保证玻璃导管的下端浸没在水中),然后(填操作方法) ,看到 (填实验现象),证明该装置的气密性良好.
(2)向试管中加入0.00127%的碘水10g,用适量的蒸馏水稀释后,再加入2~3滴淀粉溶液,配置成溶液A.测定指定地点空气中SO2的含量时,推拉注射器的活塞反复抽气,试管中发生的化学反应方程式为SO2+I2+2H2O=H2SO4+2HI,A溶液由 色变为 时表明反应恰好完全进行,此时应停止抽气.
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):一级标准:0.15;二级标准:0.50;三级标准:0.70.该课外活动小组分成第一活动小组和第二活动小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量.当反应恰好完全进行,记录抽气时间和次数如下(假定每次抽气500mL).请将下表填写完整(计算时保留2位有效数字):
①在实验过程中,需缓缓抽动活塞的目的是 ;若快速抽拉,则测定的结果将 (填偏大、偏小或无影响);
②判断该地点的空气中SO2含量属于 (填数字)级标准, (填“第一”或“第二”)小组的测定结果准确,另一小组实验结果产生较大偏差的原因是 (两个小组所用药品和装置均无问题).
查看习题详情和答案>>
| 方案 | 操作 | 结论 |
| 甲 | 分别加入到盛水的试管中 | 放热者为浓硫酸 |
| 乙 | ||
| 丙 | ||
| 丁 |

甲同学是用手捂住试管(或微热试管),观察导管中是否有液面上升的现象.是否能?
乙同学是先从玻璃导管向试管中注入水,观察导管中液面与试管中液面是否形成高度差,且在一段时间后,观察液面差是否变化的方法.是否能?
若上述两种方案均不能,请思考新方案,并填下列空白(若上述可行,则不填下列空白):先在试管中装入适量水(保证玻璃导管的下端浸没在水中),然后(填操作方法)
(2)向试管中加入0.00127%的碘水10g,用适量的蒸馏水稀释后,再加入2~3滴淀粉溶液,配置成溶液A.测定指定地点空气中SO2的含量时,推拉注射器的活塞反复抽气,试管中发生的化学反应方程式为SO2+I2+2H2O=H2SO4+2HI,A溶液由
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):一级标准:0.15;二级标准:0.50;三级标准:0.70.该课外活动小组分成第一活动小组和第二活动小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量.当反应恰好完全进行,记录抽气时间和次数如下(假定每次抽气500mL).请将下表填写完整(计算时保留2位有效数字):
| 分组 | 第一小组 | 第二小组 |
| 抽气时间 | 20分钟 | 21分钟 |
| 抽气次数 | 100 | 130 |
| SO2含量mg/m3 |
②判断该地点的空气中SO2含量属于