摘要:常温下状态:气态H2.N2.O2.F2.Cl2,液态Br2,其余为固态.晶体类型:原子晶体B.C.Si,分子晶体:除B.C.Si外的其它非金属单质.溶解性:除F2与水发生置换反应.Cl2.Br2在水中发生自身氧化还原反应外.可以说非金属单质均难溶于水.
网址:http://m.1010jiajiao.com/timu_id_284835[举报]
用NA表示阿伏加德罗常数的值,则下列叙述正确的是 ( )
A.常温下,4.48 L N2和O2的混合气体中所含原子数为0.4NA
B.常温下,1.0L 1.0 mol·L-1NaAlO2溶液中含有的氧原子数为2NA
C.7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA
D.0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.2 NA
查看习题详情和答案>>
用NA表示阿伏加德罗常数的值,则下列叙述正确的是 ( )
A.常温下,4.48 L N2和O2的混合气体中所含原子数为0.4NA
B.常温下,1.0L 1.0 mol·L-1NaAlO2溶液中含有的氧原子数为2NA
C.7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA
D.0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.2 NA
查看习题详情和答案>>
 (2009?合肥三模)A、B、C、D、E是中学常见的单质,X是化合物.A为金属,原子最外层p轨道上只有一个电子,可与NaOH溶液反应;B是常见的金属,其基态原子的外围电子排布式为3d64s2;常温下C是气态非金属单质,可以燃烧;D是空气主要成分之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:
(2009?合肥三模)A、B、C、D、E是中学常见的单质,X是化合物.A为金属,原子最外层p轨道上只有一个电子,可与NaOH溶液反应;B是常见的金属,其基态原子的外围电子排布式为3d64s2;常温下C是气态非金属单质,可以燃烧;D是空气主要成分之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:(1)写出单质B与Cl2的反应产物与X的水溶液反应的离子方程式:
Fe3++3NH3?H2O═Fe(OH)3↓+3NH4+
Fe3++3NH3?H2O═Fe(OH)3↓+3NH4+
.B单质在海水中易发生电化学腐蚀,写出电化学腐蚀的正极电极方程式:O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
.(2)已知单质E的燃烧热为296.8kJ/mol,写出表示E燃烧热的热化学方程式:
S(g)+O2(g)═SO2(g);△H=-296.8kJ/mol
S(g)+O2(g)═SO2(g);△H=-296.8kJ/mol
.(3)写出A的氧化物与NaOH溶液反应的离子方程式:
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
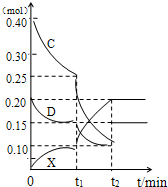
.(4)将0.40molC和0.20molD充入2L的密闭容器中,在一定条件下反应生成X,有关C、D、X三者的物质的量的变化与时间的关系如图所示:
①若t1=10min 则0~t1时间内C物质的平均反应速率为
0.0075mol/(L?min)
0.0075mol/(L?min)
;该反应平衡常数表达式为| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
②该反应在t2时达到平衡,根据图中曲线变化情况判断,t1时刻改变的反应条件可能是
a
a
(填序号)a.加入了催化剂 b.降低了反应温度 c.向容器中又充入了气体D.
A、B、C、D、E是元素周期表中前四周期常见元素,其原子序数依次增大.已知:
(1)写出A元素基态原子的价电子排布图 .当C单质、D单质和NaOH溶液形成原电池时,该原电池的负极的电极反应式为: .
(2)常温下,某气态单质甲分子与AB分子核外电子数相等,则一个甲分子中包含 个π键,在A-H、B-H两种共价键中,键的极性较强的是 (用元素符号表示).D元素原子核内中子数比质子数多1,则D原子可以表示为 ,其原子核外有 种运动状态不同的电子.
(3)B的氢化物的熔沸点比与它同主族的下一周期元素的氢化物的熔沸点高,原因是 .
(4)通常情况下,A的燃烧热为a kJ?mol-1,C的燃烧热为b kJ?mol-1,则C与AO2反应生成A的热化学方程式为 .
查看习题详情和答案>>
| A | 单质在自然界中硬度最大 |
| B | 原子中s能级与p能级电子数相等且有单电子 |
| C | C同在B的下一周期,C的电离能数据(kJ?mol-1)为:I1=738 I2=1451 I3=7732 I4=10540 |
| D | 单质密度小,较好的延展性,广泛用于食品包装,D的氧化物是两性氧化物 |
| E | 单质是一种常见金属,与O元素能形成黑色和砖红色两种氧化物 |
(2)常温下,某气态单质甲分子与AB分子核外电子数相等,则一个甲分子中包含
(3)B的氢化物的熔沸点比与它同主族的下一周期元素的氢化物的熔沸点高,原因是
(4)通常情况下,A的燃烧热为a kJ?mol-1,C的燃烧热为b kJ?mol-1,则C与AO2反应生成A的热化学方程式为
已知X、Y、Z、W为四种短周期元素,其原子序数依次增大,且由这些元素所组成的单质在常温下均呈气态.X、Y、W处于不同周期,且在一定条件下其单质能发生反应:X2+Y2→甲,X2+W2→乙,甲、乙可化合生成离子化合物丙.试回答下列问题:
(1)W元素在周期表中的位置是
(2)丙的水溶液呈酸性,用离子方程式表示其原因:
(3)X、Z可组成四原子化合物丁,丁是一种二元弱酸,写出丁在水中的电离方程式:
查看习题详情和答案>>
(1)W元素在周期表中的位置是
第三周期ⅦA族
第三周期ⅦA族
;甲的空间结构为三角锥形
三角锥形
.(2)丙的水溶液呈酸性,用离子方程式表示其原因:
NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
. NH3?H2O+H+
NH3?H2O+H+(3)X、Z可组成四原子化合物丁,丁是一种二元弱酸,写出丁在水中的电离方程式:
H2O2 H++HO2-HO2-
H++HO2-HO2- H++O22-
H++O22-
 H++HO2-HO2-
H++HO2-HO2- H++O22-
H++O22-H2O2 H++HO2-HO2-
H++HO2-HO2- H++O22-
H++O22-
;X、Y组成的液态化合物Y2X4 16克与足量丁反应生成Y2和液态水,放出Q kJ的热量,请写出该反应的热化学方程式 H++HO2-HO2-
H++HO2-HO2- H++O22-
H++O22-N2H4(l)+2H2O2(l)=N2(g)+4H2O(l);△H=-2QkJ/mol
N2H4(l)+2H2O2(l)=N2(g)+4H2O(l);△H=-2QkJ/mol
;Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极的电极反应式为N2H4-4e-+4OH-=N2+4H2O
N2H4-4e-+4OH-=N2+4H2O
.