网址:http://m.1010jiajiao.com/timu_id_284828[举报]
 根据元素周期表及周期律的知识回答下列问题:
根据元素周期表及周期律的知识回答下列问题:(1)与钠同周期且离子半径最小的元素位于周期表的第
(2)金属钠在一定条件下与氢气反应生成氢化钠(2Na+H2
| 一定条件 |
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是
a.碱性:NaOH>Mg(OH)2>Al(OH)3 b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl d.与NaOH溶液反应的剧烈程度:Na>Mg>Al
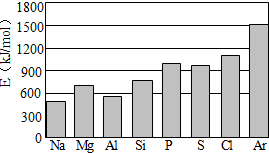
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示:
①同周期内,随着原子序数的增大,E值变化的总趋势是
②根据上图提供的信息,试推断E氟
(1)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H2
| 一定条件 |


(2)元素周期表中元素的性质存在递变规律,下列比较正确的是
a.离子半径:Na+>Mg2+>S2->Cl-b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl d.与NaOH溶液反应的剧烈程度:Na>Mg>Al
(3)共价键的极性随共用电子对偏移程度的增大而增强,SiH4、PH3、H2S、HCl共价键的极性由强到弱的顺序是
(4)元素Cl与S元素相比,非金属性较强的是
a.常温下S比Cl2单质的熔点高 b.Cl2与S的氢化物发生反应,产生S单质
c.S与Cl2形成的化合物中S元素呈正价态 d.比较两元素的单质与H2化合时得电子的数目
(5)HF比HCl沸点高,原因是
(6)下表为部分非金属元素与氢形成共价键的键长与键能数据:根据表中数据,归纳共价键键能与键长的关系
| 共价键 | H-H | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 74 | 92 | 127 | 141 | 98 | 135 | 101 | 341 |
| 键能(kJ/mol) | 436 | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
(11分)据元素周期表及周期律的知识回答下列问题:
(1)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H2 2NaH)。生成物氢化钠的电子式为__________,含有的化学键为_______键(填“离子”、“共价”或“金属”)。
2NaH)。生成物氢化钠的电子式为__________,含有的化学键为_______键(填“离子”、“共价”或“金属”)。
(2)元素周期表中元素的性质存在递变规律,下列比较正确的是____________。
a.离子半径:Na+>Mg2+>S2->Cl- b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl d.与NaOH溶液反应的剧烈程度:Na>Mg>Al
(3)共价键的极性随共用电子对偏移程度的增大而增强,SiH4、PH3、H2S、HCl共价键的极性由强到弱的顺序是_____________。
(4)元素Cl与S元素相比,非金属性较强的是_____________(用元素符号表示),下列表述中能证明这一事实的是________________
a.常温下S比Cl2单质的熔点高 b.Cl2与S的氢化物发生反应,产生S单质
c.S与Cl2形成的化合物中S元素呈正价态
d.比较两元素的单质与H2化合时得电子的数目
(5)HF比HCl沸点高,原因是___________________________________________。
(6)下表为部分非金属元素与氢形成共价键的键长与键能数据:
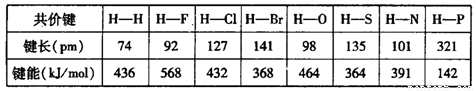
根据表中数据,归纳共价键键能与键长的关系______________________________。
查看习题详情和答案>>
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H2 2NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
2NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d.还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:
①同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
②根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H22NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d. 还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:
① 同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
② 根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
查看习题详情和答案>>