摘要:落实存在.性质.制备.用途四要点.学生活动体会“位.构.性 三者关系.[举例](1)从位置出发.以Cs为例.位置:第六周期.IA族.→结构特点:最外层只有一个电子.原子半径大.→比Na.K更活泼的金属元素.具强的金属性.→应隔绝空气保存,与水反应剧烈.可能发生爆炸,与氧气迅速反应.主要产物肯定不是Cs2O.(2)从结构出发:已知某元素原子有六个电子层.最外层2个电子→最外层电子数少.电子层数多.应是活泼金属.金属性大于钙→与水剧烈反应,氢氧化物是可溶性强碱,碳酸盐.硫酸盐均不溶于水.与教师共同分析.(3)从性质出发:某单质能从水中置换出O2.→非金属性大于氧.应为最活泼的非金属元素F→在周期表的右上角.第二周期ⅦA族→可与绝大多数金属.非金属甚至某些稀有气体直接反应,化合价只有-1价,几乎无法用氧化剂将F-氧化成F2.分析:归纳:
网址:http://m.1010jiajiao.com/timu_id_284826[举报]
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含一种金属元素。A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物甲和乙(相对分子质量甲<乙)。
请回答下列问题:
(1)写出乙的一种用途______________。
(2)用某种废弃的金属易拉罐与A、C、D组成的化合物溶液反应,所产生的气体可充填气球,请写出该反应的离子方程式___________,使用这种气球存在的隐患是_____________。
(3)已知A、B、C三种元素组成的某盐溶液常温下呈酸性,请用离子方程式表示其原因:__________。向0.02 mol·L-1的CuSO4溶液中加入由A、D、C三种元素组成的溶液来调节pH时,应使溶液的pH大于__________才能生成Cu(OH)2沉淀。[己知常温下Cu((OH)2(s) Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
(4) 在一定温度下,向一个体积为2L的密闭容器中,通入3 mol EC2和2 mol C2及固体催化剂,使之反应:2 EC2(g) + C2 (g) 2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
①加入3 mol EC2和2 mol C2发生反应,达到平衡时放出的热量为___________________。
②该温度下反应的平衡常数是________________。
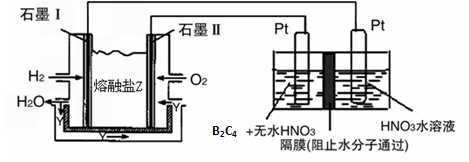
(5) B2C5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备B2C5,装置如下图所示,其中Y为CO2。写出石墨I 电极上发生反应的电极反应式 ______________。
(1)写出乙的一种用途______________。
(2)用某种废弃的金属易拉罐与A、C、D组成的化合物溶液反应,所产生的气体可充填气球,请写出该反应的离子方程式___________,使用这种气球存在的隐患是_____________。
(3)已知A、B、C三种元素组成的某盐溶液常温下呈酸性,请用离子方程式表示其原因:__________。向0.02 mol·L-1的CuSO4溶液中加入由A、D、C三种元素组成的溶液来调节pH时,应使溶液的pH大于__________才能生成Cu(OH)2沉淀。[己知常温下Cu((OH)2(s)
 Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
Cu2+(aq)+2OH-(aq), Ksp=2×10-20] (4) 在一定温度下,向一个体积为2L的密闭容器中,通入3 mol EC2和2 mol C2及固体催化剂,使之反应:2 EC2(g) + C2 (g)
 2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。①加入3 mol EC2和2 mol C2发生反应,达到平衡时放出的热量为___________________。
②该温度下反应的平衡常数是________________。
(5) B2C5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备B2C5,装置如下图所示,其中Y为CO2。写出石墨I 电极上发生反应的电极反应式 ______________。
 化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,无机非金属材料和金属材料在我们生活中有着极其广泛的用途.根据你学过的有关材料的知识,回答下列问题:
化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,无机非金属材料和金属材料在我们生活中有着极其广泛的用途.根据你学过的有关材料的知识,回答下列问题:(1)下列材料中的
①光导纤维②铝合金 ③钢铁 ④晶体硅 ⑤高温结构陶瓷
粗硅的制备是以石英和焦炭为原料在高温发生反应而制得,该反应的化学方程式为
(2)青铜是我国使用最早的合金,铜钱在我国历史上曾经是一种广泛流通的货币.下列有关铜合金的说法正确的是
A.我国较早的掌握了湿法冶炼钢的技术
B.铜的性质不活泼,自然界有大量的游离态的铜
C.常见的铜合金除了青铜外还有黄铜和白铜
D.铜常用于制造货币的原因是铜合金的熔点较低,易于冶炼、铸造成型,且不易被腐蚀
(3)“纳米材料”是粒子直径为1nm~100nm的材料,纳米碳就是其中的一种.某研究所将纳米碳均匀的分散到蒸馏水中,得到的分散系:①是溶液 ②是胶体 ③具有丁达尔现象 ④不能透过滤纸 ⑤不能透过半透膜 ⑥静止后会出现黑色沉淀.其中正确的是
许多元素都存在同位素,目前已发现的110多种元素中,稳定同位素约300种,而放射性同位素达1 500种以上,而且大多数是人工制备的。同位素在生产、生活和科研中有着十分广泛的用途,比如:测定矿石、生物遗体的年代,研究反应机理,优良育种、临床治癌,核动力发电等。完成下列有关同位素的问题的填空。
(1)物质的量的单位摩尔是以________________所含的原子个数为标准。
(2)
相对分子质量为248的A·5H2O是无色透明晶体,无臭,味咸,在纺织工业中用于棉织品漂白后的脱氯剂等用途。甲是淡黄色固体、不溶于水,易溶于二硫化碳;乙、丙是气体,反应①可以制取三种重要的化工原料,乙可与E反应;D 是形成酸雨的污染物,F是过量的E与D反应后的物质。如图是关于A及相关物质性质与制备A的相互转化关系。

(1)写出E的电子式:________,组成乙的元素原子结构示意图是________,反应②的条件是___________。
(2)写出反应①电解的阴极电极反应式:_____________ 。
(3)写出A与B溶液反应的离子方程式:_______________。
(4)写出甲与F溶液反应制备A的化学方程式:_______________。
查看习题详情和答案>>
(2)写出反应①电解的阴极电极反应式:_____________ 。
(3)写出A与B溶液反应的离子方程式:_______________。
(4)写出甲与F溶液反应制备A的化学方程式:_______________。