摘要:C. Pt为正极.其电极反应为:
网址:http://m.1010jiajiao.com/timu_id_272022[举报]
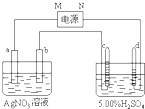 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,只在c、d两极上共收集到336mL(标准状态)气体.回答:
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,只在c、d两极上共收集到336mL(标准状态)气体.回答:(1)直流电源中,M为
正
正
极.(2)Pt电极上生成的物质是
银
银
,其质量为2.16
2.16
g.(3)请写出C电极的电极反应式
4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
.(4)AgNO3溶液的浓度(填增大、减小或不变.下同)
不变
不变
,H2SO4溶液的pH减小
减小
.(5)H2SO4溶液质量分数由5.00%变为5.02%,则原5.00% H2SO4溶液为
45.18
45.18
g.用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO4)=1:9]。t1时刻a电极得到混合气体,其中Cl2在标准状况下为224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是( )
A.a电极与电源的负极相连
B.t2时,两电极的质量相差3.84 g
C.电解过程中,溶液的pH不断增大
D.t2时,b的电极反应是4OH-一4e-=2H2O+O2↑
查看习题详情和答案>>
