网址:http://m.1010jiajiao.com/timu_id_270167[举报]
一、单项选择题(本题包括12小题,每小题4分,共48分。每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
D
A
B
A
C
B
D
C

 22.(14分)
(1) O、H、S、Cl 硫酸(4分)
22.(14分)
(1) O、H、S、Cl 硫酸(4分)
(2) (3分)
(3) SO2 + 2H2O + Cl2 = 4H++ SO42-+ 2Cl-(3分)
SO2和Cl2按相等物质的量通入品红溶液(2分)
(4) Fe + S
 FeS,2Fe + 3Cl2
FeS,2Fe + 3Cl2
 2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
或Cl2 + Na2S S↓+ 2NaCl)(2分)
四、实验题(本大题共2小题,共21分)
23.(5分)
(1)同周期
(2)同主族
Ⅰ
A、F、H
E、D
Ⅱ
d、c、b
g、f
24.(16分) (1) 分液漏斗上口的塞子未打开(或漏斗未与大气相通或漏斗塞子的凹槽未与颈部的通气孔对准。(2分)
(2) ④ (2分)
(3) 溶液由红色褪为无色,SO2 + OH- = HSO3-或SO2 + 2OH-= SO32-+ H2O。 (4分)
(4) 产生白色沉淀,SO2被HNO3氧化产生SO42-,与Ba2+产生白色沉淀。(4分)
(5) ① 关闭K2,在烧杯中用水封住玻璃导管口,用手捂住集气瓶b,烧杯中导管口有气泡产生,松手后,导管内有一段液柱保持不降则气密性好。(2分)
② 打开K1,关闭K2,点燃酒精灯。(2分)
五、计算题(本大题共1个小题,共11分)
25.(1) S H2S Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S↓+ H2O
Na2S + H2SO4 = Na2SO4 + H2S↑ 2H2S+SO2=3S↓+2H2O(各1分)
(2) Na2S2O3 :0.025 mol Na2S:0.075 mol(各3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
A、B、C、D、E、F、G、H八种前四周期元素,原子序数依次增大,化合物甲由A、D、E三种元素组成,常温下0.1mol/L甲溶液的pH=13;B、F同主族,F是重要的半导体材料。G为前四周期单电子数最多的元素,H最外层电子数与G相同。
(1)G的元素符号是_________原子的价电子排布图为______________
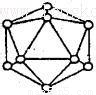
(2)短周期元素I与F性质相似,晶体类型相同,基本单元如图所示,可表示为I12,则其基本结构中含有正三角形的个数为____________
(3)C与其同族相邻元素J所形成的简单气态氢化物键角大小关系_______________(用 化学式表示)原因_____________________________
(4)B与D两元素组成的常见无机粒子中,其空间构型可能是 (填写序号)。
a.直线型 b.平面三角形 c.三角锥形 d.正四面体
(5)H原子晶体堆积模型为________________,若其密度为ρg/cm3 阿伏伽德罗常数为NA,求最近两个H原子间的距离为_________________pm(列出计算式)
查看习题详情和答案>>
(1)G的元素符号是_________原子的价电子排布图为______________
(2)短周期元素I与F性质相似,晶体类型相同,基本单元如图所示,可表示为I12,则其基本结构中含有正三角形的个数为____________

(3)C与其同族相邻元素J所形成的简单气态氢化物键角大小关系_______________(用 化学式表示)原因_____________________________
(4)B与D两元素组成的常见无机粒子中,其空间构型可能是 (填写序号)。
a.直线型 b.平面三角形 c.三角锥形 d.正四面体
(5)H原子晶体堆积模型为________________,若其密度为ρg/cm3 阿伏伽德罗常数为NA,求最近两个H原子间的距离为_________________pm(列出计算式)
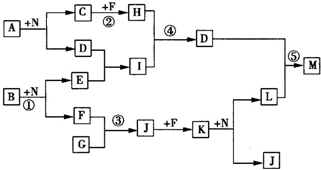 如右框图反应中所涉及的l4种物质都是由短周期元素组成的.已知:
如右框图反应中所涉及的l4种物质都是由短周期元素组成的.已知:(Ⅰ)F为单质;
(Ⅱ)A、B、C、G、H、J、K、N均是由两种元素组成的化合物,且C、G为同周期元素形成的简单气态氢化物;
(Ⅲ)D、E、I、L、M均是由3种元素组成的化合物,且D具有两性;
(Ⅳ)反应中生成的水均已略去.
请回答下列问题:
(1)写出化学式:B
(2)写出E的电子式:
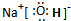
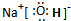
(3)反应③的化学方程式为
| ||
| △ |
| ||
| △ |
(4)解释反应⑤中生成的M的水溶液呈酸性的原因:
(5)反应②中,每1.00g C与足量的F作用,恢复到25℃时放出55.6kJ的热量,写出反应②的热化学方程式:
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。对于所示元素下列叙述中正确的是

A.f、i、l形成的简单离子所带电荷数值与其族序数相等
B.b与h、j、g形成的化合物每个分子均含有10个电子
C.B所在的区域全是过渡元素,它们的单质或化合物在日常生活中都很难见到
D.最高价氧化物对应水化物碱性:nOH > d(OH)2 > f(OH)3
查看习题详情和答案>>| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | ||||||||||||||
| K | M | L |
(1)写出上表中元素D形成单质的电子式为


(2)元素K基态原子的电子排布式


(3)元素M位于周期表的第
(4)G、H、I 这三种元素的第一电离能由大到小的顺序是
(5)元素A、D、J按照原子个数比4:1:1形成的化合物的化学式为
(6)A、C、D 形成的ACD分子中,含有
(7)E、F、G、H这四种元素原子形成的简单阴、阳离子,按半径由小到大排列
(8)某些不同族元素的性质也有一定的相似性,如上表中元素B与元素I的氢氧化物有相似的性质,写出元素B的氢氧化物与NaOH溶液反应后盐的化学式
(9)元素L在一定条件下形成的晶体的基本结构单元如图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:
