摘要:(1)HCO3- + H2O H2CO3 + OH---大于-- (3)==.>--
网址:http://m.1010jiajiao.com/timu_id_249692[举报]
写出下列化学反应的离子方程式
(1)NaHCO3与HCl
(2)NaHCO3与NaOH
查看习题详情和答案>>
(1)NaHCO3与HCl
HCO3-+H+=H2O+CO2↑
HCO3-+H+=H2O+CO2↑
;(2)NaHCO3与NaOH
HCO3-+OH-=H2O+CO32-
HCO3-+OH-=H2O+CO32-
. 钠与水反应的过程如图所示.请回答:
钠与水反应的过程如图所示.请回答:(1)钠与水反应的化学方程式为
2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
.(2)根据B中的实验现象,说明钠的密度比水的
小
小
(填“大”或“小”).(3)C中滴加酚酞试液后,可观察到溶液变
红
红
色.(4)在实验室中通常将钠保存在
煤油
煤油
里(填序号).①冷水 ②煤油(5)现有A、B、C三种白色固体及一种无色气体D.A、B、C均可溶于水,焰色反应均呈黄色,其中C的溶液为碱溶液,且四种物质之间存在如下关系:
①A+D+H2O→B ②B+C→A+H2O
③C+D→A+B ④B
| △ |
请回答:A是
Na2CO3
Na2CO3
,D是CO2
CO2
(写化学式);反应②的离子方程式是HCO3-+OH-=CO32-+H2O
HCO3-+OH-=CO32-+H2O
;少量D通入C的离子方程式是3OH-+2CO2=HCO3-+CO32-+H2O
3OH-+2CO2=HCO3-+CO32-+H2O
;反应④的化学方程式是2NaHCO3=Na2CO3+CO2+H2O
2NaHCO3=Na2CO3+CO2+H2O
.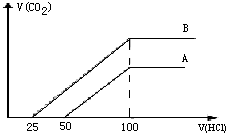 取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示.
取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示.(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式)
Na2CO3
Na2CO3
加入盐酸后产生CO2体积的最大值112
112
ml,滴入盐酸的过程中发生反应的离子方程式CO32-+H+=HCO3-
CO32-+H+=HCO3-
、HCO3-+H+=H2O+CO2↑
HCO3-+H+=H2O+CO2↑
.(2)曲线B 表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式)
Na2CO3、NaHCO3
Na2CO3、NaHCO3
,两溶质物质的量之比为1:2
1:2
;加入盐酸后产生CO2体积的最大值为168
168
ml.(3)求原NaOH溶液物质的量的浓度
0.5
0.5
mol?L-1.(2011?武胜县一模)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子最外层电子数与次外层电子数之比为3:4;N-、Z+、X+离子的半径逐渐减小;化合物XN为分子晶体.据此回答:
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式)
(2)用X的三种同位素与16O、18O构成的X2O所有分子,其相对分子质量的数值有
(3)已知通常状况下1g X2在Y2中完全燃烧放出a kJ的热量,请写出表示X2燃烧热的热化学方程式
(4)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式
(5)化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1:1:1,A溶液中水的电离程度比在纯水中小.则化合物A中的化学键类型为
 .
.
(6)向1.5L 0.1mol?L-1 Z的最高价氧化物对应水化物的水溶液中通入标况下2.24L CO2,充分反应.离子方程式是
查看习题详情和答案>>
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式)
HClO4
HClO4
.(2)用X的三种同位素与16O、18O构成的X2O所有分子,其相对分子质量的数值有
7
7
种.(3)已知通常状况下1g X2在Y2中完全燃烧放出a kJ的热量,请写出表示X2燃烧热的热化学方程式
H2(g)+
O2(g)═H2O(l);△H=一2akJ?mol-1
| 1 |
| 2 |
H2(g)+
O2(g)═H2O(l);△H=一2akJ?mol-1
.| 1 |
| 2 |
(4)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式
H2O2+H2S═S↓+2H2O
H2O2+H2S═S↓+2H2O
.(5)化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1:1:1,A溶液中水的电离程度比在纯水中小.则化合物A中的化学键类型为
离子键、极性键
离子键、极性键
;若B为常见家用消毒剂的主要成分,则B的电子式是

(6)向1.5L 0.1mol?L-1 Z的最高价氧化物对应水化物的水溶液中通入标况下2.24L CO2,充分反应.离子方程式是
2CO2+3OH-﹦HCO3-+CO32-+H2O
2CO2+3OH-﹦HCO3-+CO32-+H2O
.氯气是一种重要的工业原料.
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4
2CaSO4+2Cl2↑+2H2O
他们利用该反应设计如下制取氯气并验证其性质的实验.
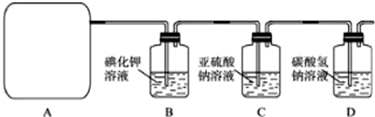
回答下列问题:
(1)该实验中A部分的装置是
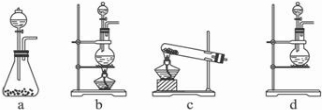
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):
(3)写出D装置中发生反应的离子方程式
(4)该实验存在明显的缺陷,请你提出改进的方法
(5)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1mol?L-1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI,共用去Na2S2O3溶液20.0mL.则该漂白粉中Ca(ClO)2的质量分数为
查看习题详情和答案>>
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4
| ||
他们利用该反应设计如下制取氯气并验证其性质的实验.

回答下列问题:
(1)该实验中A部分的装置是
b
b
(填标号).
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):
取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化
取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化
.(3)写出D装置中发生反应的离子方程式
Cl2+H2O═H++Cl-+HClO;H++HCO3-═CO2↑+H2O
Cl2+H2O═H++Cl-+HClO;H++HCO3-═CO2↑+H2O
.(4)该实验存在明显的缺陷,请你提出改进的方法
应将尾气通入NaOH溶液中
应将尾气通入NaOH溶液中
.(5)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1mol?L-1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI,共用去Na2S2O3溶液20.0mL.则该漂白粉中Ca(ClO)2的质量分数为
35.75%
35.75%
.