摘要:B.研究质子和中子的结构是化学科学研究的一项新任务
网址:http://m.1010jiajiao.com/timu_id_245695[举报]
必考卷
第Ⅰ卷
一、选择题:每小题3分,共45分
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
A
C
D
C
C
D
B
A
B
B
A
A
D
D
C
第Ⅱ卷
二、填空题:
16.(10分)
每空2分,化学方程式、离子方程式没有配平不给分,条件未标扣1分,沉淀、气体符
号未标不扣分。
(1)O
(2)
(3)


(4)
(5)O=C=O
17.(10分)
每空2分,化学方程式、离子方程式没有配平不给分,条件未标扣1分,沉淀、气体符
号未标不扣分。
(1) 
(2)第三周期第ⅥA族
(3)氧,B
(4)
18.(12分)
实验一
(1)胶头滴管、250mL容量瓶 (每空1分,共2分)
(2)0.2000mol?L (2分)
(2分)
实验二
(1)0.0100mo1?L 醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于l
醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于l
(3分,其它合理答案酌情给分)
(2)增大 、(2分)
实验三
答:用pH计(或pH试纸)测定相同浓度的醋酸在几种不同'温度时的pH(3分其他合
19.(10分)
每空2分,其它合理答案酌情给分
(1)
(2)CD
(3)
(4)甲醇、氢氧化钠、水(答出甲醇即给2分) 
选考卷
20(A).(13分)
(1)分子晶体 (2分)
(2)没有 (2分)
(3) .
(3分)
.
(3分)
(4)O N C (2分)
(5) 键和
键和 键 (2分)
键 (2分)
(6)CO中断裂第一个 键消耗的能量(273
kJ?mol
键消耗的能量(273
kJ?mol )比N
)比N 中断裂第一个
中断裂第一个 键消耗的能量(523.3kJ?mol
键消耗的能量(523.3kJ?mol )小,CO的第一个键较容易断裂,因此CO较活泼。(其它合理答案酌情给分)(2分)
)小,CO的第一个键较容易断裂,因此CO较活泼。(其它合理答案酌情给分)(2分)
20(B).(13分)
(1)羟基,羧基(2分)
(2)消去反应(2分)
(3) 
(4) 
(5) 4 (2分)
(6) 
[化学-物质结构与性质]
研究物质结构是为更好的掌握物质的性质.
(1)第四周期过渡元素在性质上存在一些特殊性,在前沿科技中应用广泛.
①铜为第四周期过渡元素,其基态原子电子排布式为
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
③在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有
(2)已知:下表是14种元素的电负性的数值(用X表示).
①经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键,如NaCl;当小于1.7时,一般为共价键,如AlCl3.请写出铁元素和表中非金属元素形成的常见共价化合物:
②气态氯化铝通常以二聚分子形式存在,分子式为Al2Cl6,分子中所有原子均达到8电子稳定结构,则Al2Cl6的结构式为
 .
.
③由表中两种元素形成的化合物中,分子中既含有σ键又含有π键,且二者数目相同的有(写一个即可)
查看习题详情和答案>>
研究物质结构是为更好的掌握物质的性质.
(1)第四周期过渡元素在性质上存在一些特殊性,在前沿科技中应用广泛.
①铜为第四周期过渡元素,其基态原子电子排布式为
[Ar]3d104s1
[Ar]3d104s1
,请解释金属铜能导电的原因铜是由自由电子和金属阳离子通过金属键形成,自由电子在外电场中可以定向移动,所以能导电.
铜是由自由电子和金属阳离子通过金属键形成,自由电子在外电场中可以定向移动,所以能导电.
.②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列
bc
bc
.a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
③在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有
离子键、配位键
离子键、配位键
.(2)已知:下表是14种元素的电负性的数值(用X表示).
| 元素 | Al | B | Be | C | Cl | F | Li |
| X | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | Fe |
| X | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | 1.8 |
FeCl3或FeS
FeCl3或FeS
.②气态氯化铝通常以二聚分子形式存在,分子式为Al2Cl6,分子中所有原子均达到8电子稳定结构,则Al2Cl6的结构式为


③由表中两种元素形成的化合物中,分子中既含有σ键又含有π键,且二者数目相同的有(写一个即可)
CO2或CS2
CO2或CS2
,其分子空间构型为直线型
直线型
.[化学-选修/物质结构与性质]
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于 .
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为 .
(2)下表为元素周期表的一部分,根据此表回答下列问题:
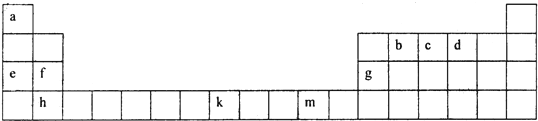
①f、g、h三种元素的第一电离能由小到大的顺序是 (用元素符号表示),b、c、d三种元素的电负性由大到小的顺序是 (用元素符号表示),b、c、d分别与a形成的简单化合物分子中,属于含有极性键的非极性分子是 .(填写化学式)
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式 .
目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为 .
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
,其中各原子的最外层电子均满足8电子稳定结构.该阴离子的中心原子的杂化轨道方式为 杂化,阴离子的电子式为 .
查看习题详情和答案>>
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为
(2)下表为元素周期表的一部分,根据此表回答下列问题:

①f、g、h三种元素的第一电离能由小到大的顺序是
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式

目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
3- 4 |
化学上通常把原子数和电子数相等的分子或离子称为等电子体,研究发现等电子体间结构和性质相似(等电子原理).化合物B3N3H6被称为无机苯,它与苯是等电子体,则下列说法中不正确的是( )
| A、无机苯是仅由极性键组成的分子 | B、无机苯能发生加成反应和取代反应 | C、无机苯的二氯代物有3种同分异构体 | D、无机苯不能使酸性KMnO4溶液褪色 |
[化学──选修物质结构与性质]
图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中第一电离能最小的是: (填编号).比元素B原子序数大10的元素在元素周期表中的位置: 周期, 族,其基态原子的核外电子排布是 .
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是 (写分子式,写出两种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 .
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成 个σ键, 个π键.
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第 族.

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第 族元素氢化物的沸点的变化规律.不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线-折线a和折线b,你认为正确的是 ,理由是 .
查看习题详情和答案>>
图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 |
A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中第一电离能最小的是:
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第