摘要:方法2.先做转换2只需比较A为CH4.B.C相同为C2H2.D转化为C2H4.耗氧
网址:http://m.1010jiajiao.com/timu_id_237624[举报]
(2013?盐城一模)多晶硅是太阳能光伏产业的重要原材料.
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)═SiO(g)+CO(g),△H=akJ?mol-1
2SiO(g)═Si(s)+SiO2(s),△H=bkJ?mol-1
①反应SiO2(s)+2C(s)═Si(s)+2CO(g)的△H=
②SiO是反应过程中的中间产物,隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为
(2)粗硅提纯常见方法之一是先用粗硅与HCl反应,制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g).不同温度及不同
时,反应物X的平衡转化率关系如图1.
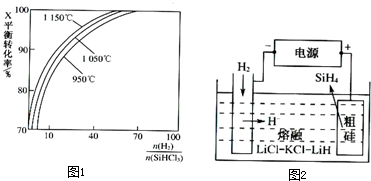
①X是
②上述反应的平衡常数:K(1150℃)
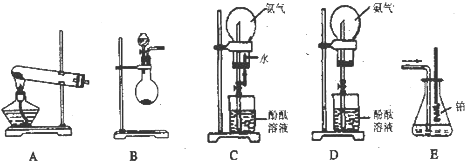
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法.
①用粗硅做原料,熔盐电解法制取硅烷原理如图2所示,电解时阳极的电极反应式为
②硅基太阳能电池需用N、Si两种元素组成的化合物Y做钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到.已知Y中Si的质量分数为60%,Y的化学式为
查看习题详情和答案>>
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)═SiO(g)+CO(g),△H=akJ?mol-1
2SiO(g)═Si(s)+SiO2(s),△H=bkJ?mol-1
①反应SiO2(s)+2C(s)═Si(s)+2CO(g)的△H=
2a+b
2a+b
kJ?mol-1(用含a、b的代数式表示);②SiO是反应过程中的中间产物,隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为
SiO+2NaOH═Na2SiO3+H2
SiO+2NaOH═Na2SiO3+H2
.(2)粗硅提纯常见方法之一是先用粗硅与HCl反应,制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g).不同温度及不同
| n(H2) | n(SiHCl3) |

①X是
SiHCl3
SiHCl3
(填化学式);②上述反应的平衡常数:K(1150℃)
>
>
K(950℃)(填“>”、“<”或“=”).(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法.
①用粗硅做原料,熔盐电解法制取硅烷原理如图2所示,电解时阳极的电极反应式为
Si+4H+-4e-═SiH4↑
Si+4H+-4e-═SiH4↑
.②硅基太阳能电池需用N、Si两种元素组成的化合物Y做钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到.已知Y中Si的质量分数为60%,Y的化学式为
Si3N4
Si3N4
. 某校学习小组进行下述实验探究乙酸、碳酸和苯酚的酸性强弱关系该校学生设计了如图的实验装置(夹持仪器已略去).
某校学习小组进行下述实验探究乙酸、碳酸和苯酚的酸性强弱关系该校学生设计了如图的实验装置(夹持仪器已略去).(1)某学生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否?
正确
正确
(填“正确”或“错误”),大理石与乙酸溶液反应的化学方程式为CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O
CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为
试管内溶液出现浑浊
试管内溶液出现浑浊
反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-
C6H5O-+CO2+H2O→C6H5OH+HCO3-
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是:
在装置A和B之间连一个盛有饱和氢钠溶液的洗气瓶
在装置A和B之间连一个盛有饱和氢钠溶液的洗气瓶
. 实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:
实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中除了加入
乙醇
乙醇
、浓硫酸
浓硫酸
、乙酸
乙酸
外,还应放入几块碎瓷片,其目的是防止烧瓶中液体暴沸.(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:
先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
.(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,当达到化学平衡状态时:(填序号)
②④⑤
②④⑤
.①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等 ⑤混合物中各物质的浓度不再变化
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图.请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法.

E为
乙醇
乙醇
(填名称);试剂a是饱和碳酸钠溶液
饱和碳酸钠溶液
,试剂b为浓硫酸
浓硫酸
;分离方法①是分液
分液
,分离方法②是蒸馏
蒸馏
.(5)写出合成乙酸乙酯反应的化学方程式
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| 加热 |
CH3COOH+C2H5OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| 加热 |
(2010?宝鸡二模)下列图示是学生课外活动小组设计的制取氨气并进行氨气溶于水的喷泉实验等实验的装置示意图.
请回答下列问题:
(1)学生甲用图A所示装置制备氨气,写出该法制取氨气的化学方程式
制出的氨气应使用
(2)学生乙用图B所示装置也制出了氨气,他选用的制取试剂可能是
(3)学生丙用图C所示装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是:
(4)学生丁将装置C误装为装置D,但经同学讨论后,认为也可引发喷泉.请说明用该装置引发喷泉的方法:
(5)学生戊用装置E吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入戊装置的锥形瓶内,看到了具有催化作用的铂丝保持红热,同时瓶内生成了红棕色的气体.写出在此过程中可能发生反应的化学方程式:
查看习题详情和答案>>

请回答下列问题:
(1)学生甲用图A所示装置制备氨气,写出该法制取氨气的化学方程式
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
;
| ||
制出的氨气应使用
向下排空气
向下排空气
法来收集,要得到干燥的氨气可选用碱石灰
碱石灰
做干燥剂.(2)学生乙用图B所示装置也制出了氨气,他选用的制取试剂可能是
氧化钙
氧化钙
和氢氧化钠
氢氧化钠
.(3)学生丙用图C所示装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是:
打开止水夹,挤出胶头滴管中的水
打开止水夹,挤出胶头滴管中的水
.(4)学生丁将装置C误装为装置D,但经同学讨论后,认为也可引发喷泉.请说明用该装置引发喷泉的方法:
打开止水夹,用手(或热毛巾等)将烧瓶捂热,氨受热膨胀,赶出玻璃导管中的空气,氨气与水接触,即发生喷泉
打开止水夹,用手(或热毛巾等)将烧瓶捂热,氨受热膨胀,赶出玻璃导管中的空气,氨气与水接触,即发生喷泉
(5)学生戊用装置E吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入戊装置的锥形瓶内,看到了具有催化作用的铂丝保持红热,同时瓶内生成了红棕色的气体.写出在此过程中可能发生反应的化学方程式:
4NH3+5O2
4NO+6H2O,2NO+O2═2NO2
| ||
| △ |
4NH3+5O2
4NO+6H2O,2NO+O2═2NO2
.
| ||
| △ |