摘要:(3)NaN3, CO2 N2O BeF2, (4)增大
网址:http://m.1010jiajiao.com/timu_id_236640[举报]
已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为75%,C、J是同周期元素的气态氢化物,X为无色液体,D具有两性.反应生成的水均已略去.它们有如下图所示的关系.

(1)写出化学式:A.
(2)反应③中每生成lmolF,转移电子的数目为:
(3)反应④的化学方程式为:
(4)写出离子方程式分别为:反应②
反应⑤
(5)反应①中,每1.00g C与足量的F作用,恢复到25℃放出55.6kJ热量,写出反应①的热化学方程式.
查看习题详情和答案>>

(1)写出化学式:A.
Al4C3
Al4C3
,B.Na2O2
Na2O2
,C.CH4
CH4
.(2)反应③中每生成lmolF,转移电子的数目为:
1.204×1024
1.204×1024
.(3)反应④的化学方程式为:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(4)写出离子方程式分别为:反应②
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-
;反应⑤
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
.(5)反应①中,每1.00g C与足量的F作用,恢复到25℃放出55.6kJ热量,写出反应①的热化学方程式.
CH4(g)+2O2(g)
CO2(g)+2H2O(l);△H=-889.6kJ?mol-1
| ||
CH4(g)+2O2(g)
CO2(g)+2H2O(l);△H=-889.6kJ?mol-1
.
| ||
某化学兴趣小组以含铁的废铝为原料制备硫酸铝晶体,设计如下的实验方案:请回答以下问题:

(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有
(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净:
(3)评价步骤②的操作中难以控制之处
(4)步骤①中使用的NaOH溶液以4mol/L为宜.某同学称量mgNaOH固体配制V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)
查看习题详情和答案>>

(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有
烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
;(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净:
取最后一次洗涤液,加入几滴BaCl2溶液,若无白色沉淀生成则洗涤干净
取最后一次洗涤液,加入几滴BaCl2溶液,若无白色沉淀生成则洗涤干净
;(3)评价步骤②的操作中难以控制之处
使溶液的pH=8~9难以控制
使溶液的pH=8~9难以控制
,请你提出一个合理而比较容易操作的实验方案(药品可任选)通入过量CO2气体
通入过量CO2气体
,该反应的分子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
;(4)步骤①中使用的NaOH溶液以4mol/L为宜.某同学称量mgNaOH固体配制V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)
①④⑤
①④⑤
.某强酸性溶液X可能含有Ba2+、Al3+、N
、Fe2+、Fe3+、C
、S
、S
、Cl-、N
、N
中的一种或几种,取该溶液进行连续实验,实验过程如下:
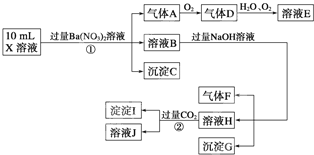
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
(2)沉淀I的化学式为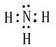
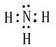 .
.
(3)写出反应②的离子方程式:
(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式
(5)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有
查看习题详情和答案>>
| H | + 4 |
| O | 2- 3 |
| O | 2- 3 |
| O | 2- 4 |
| O | - 2 |
| O | - 3 |

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
Al3+、NH4+、Fe2+、SO42-
Al3+、NH4+、Fe2+、SO42-
,不能确定是否含有的离子(M)是Fe3+、Cl-
Fe3+、Cl-
,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是取少量X溶液于试管中,加入几滴KSCN溶液不变红色则说明无Fe3+;或取少量B溶液少许于试管中,加几滴AgNO3溶液,若无白色沉淀说明无Cl-
取少量X溶液于试管中,加入几滴KSCN溶液不变红色则说明无Fe3+;或取少量B溶液少许于试管中,加几滴AgNO3溶液,若无白色沉淀说明无Cl-
.(2)沉淀I的化学式为
Al(OH)3
Al(OH)3
,气体F的电子式为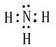
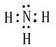
(3)写出反应②的离子方程式:
AlO2-+CO2+H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+H2O=Al(OH)3↓+HCO3-
.(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式
3ClO-+2Fe(OH)3+4OH-=3Cl-+FeO42-+5H2O
3ClO-+2Fe(OH)3+4OH-=3Cl-+FeO42-+5H2O
.(5)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有
Fe3+
Fe3+
.某待测液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH 4+

等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的).
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由.答:
(2)写出沉淀D的分子式:
(3)写出从溶液D生成沉淀E的反应的离子方程式:
查看习题详情和答案>>

等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的).
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由.答:
含有Ba2+、Ca2+离子中的一种或两种,因为BaSO4不溶于水,CaSO4微溶于水
含有Ba2+、Ca2+离子中的一种或两种,因为BaSO4不溶于水,CaSO4微溶于水
.(2)写出沉淀D的分子式:
Fe(OH)3
Fe(OH)3
.(3)写出从溶液D生成沉淀E的反应的离子方程式:
CO2+3H2O+2AlO2-═2Al(OH)3↓+2CO32-或CO2+2H2O+AlO2-═Al(OH)3↓+2HCO3-,
CO2+3H2O+2AlO2-═2Al(OH)3↓+2CO32-或CO2+2H2O+AlO2-═Al(OH)3↓+2HCO3-,
.