摘要:总反应式:2HCl H2↑+Cl2↑(2)KOH 阳极:4OH--4e→2H2O+O2↑阴极:4H++4e→2H2↑
网址:http://m.1010jiajiao.com/timu_id_234218[举报]
如图甲、乙是电化学实验装置.有关电极反应或计算错误的是( )

A.若甲烧杯中盛有NaCl溶液,则石墨棒上的电极反应式为O2+2H2O+4e-═4OH-
B.若乙烧杯中盛有NaCl溶液,则乙中的总反应为2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.若甲烧杯中盛有CuSO4溶液,则甲中铁棒上的电极反应式为Fe-2e-═Fe2+
D.若起始时乙中盛有200 mL pH=5的CuSO4溶液,一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入0.6g CuO
查看习题详情和答案>>

A.若甲烧杯中盛有NaCl溶液,则石墨棒上的电极反应式为O2+2H2O+4e-═4OH-
B.若乙烧杯中盛有NaCl溶液,则乙中的总反应为2Cl-+2H2O
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑C.若甲烧杯中盛有CuSO4溶液,则甲中铁棒上的电极反应式为Fe-2e-═Fe2+
D.若起始时乙中盛有200 mL pH=5的CuSO4溶液,一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入0.6g CuO
查看习题详情和答案>>
第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.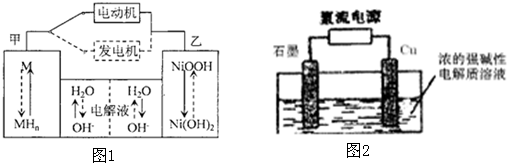
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH
(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
Cu2O+H2阴极的电极反应式是
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
查看习题详情和答案>>

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g),△H=-5121.9KJ/mol
| 25 |
| 2 |
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g),△H=-5121.9KJ/mol
.| 25 |
| 2 |
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
| 放电 |
| 充电 |
增大
增大
(填“增大”、“减小”或“不变”),该电极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-
NiOOH+H2O+e-=Ni(OH)2+OH-
.(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
| ||
2H++2e-=H2↑
2H++2e-=H2↑
.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为144
144
g.(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
吸氧
吸氧
腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的负
负
极(填“正”或“负”)相连. 混合动力车的电动机目前一般使用的是镍氢电池,在上坡或加速时,电池处于放电状态,
混合动力车的电动机目前一般使用的是镍氢电池,在上坡或加速时,电池处于放电状态,在刹车或下坡时电池处于充电状态.镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理如图,其总反应式为:
H2+2NiOOH
 2Ni(OH)2
2Ni(OH)2下列有关混合动力车的判断正确的是( )
查看习题详情和答案>>
 (2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
(2010?江苏二模)近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1mol水蒸气放热569.1kJ.则该反应的热化学方程式为
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g)△H=-5121.9kJ?mol-1
| 25 |
| 2 |
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g)△H=-5121.9kJ?mol-1
.| 25 |
| 2 |
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理示意如图,其总反应式是:H2+2NiOOH
| 放电 |
| 充电 |
增大
增大
(填“增大”、“不变”或“减小”),该电极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-
NiOOH+H2O+e-=Ni(OH)2+OH-
.(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g)+
| 1 |
| 2 |
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
| 容器编号 | c(CO)/mol?L-1 | c (02)/mol?L-1 | c (C02)/mol?L-1 | v(正)和v (逆)比较 |
| I | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 |
1.1×10-6
1.1×10-6
mol?L-1.镍及其化合物与生产、生活密切相关.
(1)镍能与CO反应,生成的Ni(CO)4受热易分解,化学方程式为:Ni(s)+4CO(g)?Ni(CO)4(g)
①该反应的正反应为 (填“吸热”或“放热”)反应.
②吸烟时,烟草燃烧生成的CO会与烟草中微量的Ni在肺部发生该反应,生成容易进入血液的Ni(CO)4,使人重金属中毒.从化学平衡的角度分析,促使Ni(CO)4在血液中不断分解的原因是 .
③镍与CO反应会造成镍催化剂中毒.为防止镍催化剂中毒,工业上常用SO2除CO.已知:
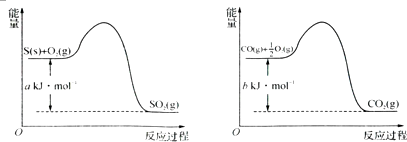
则用SO2除去CO的热化学方程式为 .
(2)为了研究镍制备过程中的各种因素对镍催化剂损耗的影响,选择制造镍催化剂的条件有:干燥方式为喷雾干燥、烘箱干燥,粒度大小为40μm和55μm,实验温度为60℃和80℃.设计下表实验,填写下列空白:
(3)混合动力车通常使用碱性镍氢充放电池,其总反应式为:H2+2NiOOH
2Ni(OH)2
①混合动力车在刹车或下坡时,电池处于充电状态,此时阳极的电极反应式 ;
②镍氢电池材料(NiOOH)可在氢氧化钠溶液中用NaClO氧化NiSO4制得,该反应的化学方程式为 .
查看习题详情和答案>>
(1)镍能与CO反应,生成的Ni(CO)4受热易分解,化学方程式为:Ni(s)+4CO(g)?Ni(CO)4(g)
①该反应的正反应为
②吸烟时,烟草燃烧生成的CO会与烟草中微量的Ni在肺部发生该反应,生成容易进入血液的Ni(CO)4,使人重金属中毒.从化学平衡的角度分析,促使Ni(CO)4在血液中不断分解的原因是
③镍与CO反应会造成镍催化剂中毒.为防止镍催化剂中毒,工业上常用SO2除CO.已知:

则用SO2除去CO的热化学方程式为
(2)为了研究镍制备过程中的各种因素对镍催化剂损耗的影响,选择制造镍催化剂的条件有:干燥方式为喷雾干燥、烘箱干燥,粒度大小为40μm和55μm,实验温度为60℃和80℃.设计下表实验,填写下列空白:
| 实验编号 | T/℃ | 颗粒大小/μm | 干燥方式 | 实验目的 |
| 1 | 60 | 40 | 烘箱干燥 | (Ⅰ)实验1和2制得的镍催化剂,用于探究制备的干燥方式对镍催化剂损耗的影响 (Ⅱ)实验1和3制得的镍催化剂,用于探究制备的制备温度对镍催化剂损耗的影响 (Ⅲ) |
| 2 | ||||
| 3 | ||||
| 4 | 60 | 55 | 烘箱干燥 |
| 放电 |
| 充电 |
①混合动力车在刹车或下坡时,电池处于充电状态,此时阳极的电极反应式
②镍氢电池材料(NiOOH)可在氢氧化钠溶液中用NaClO氧化NiSO4制得,该反应的化学方程式为