摘要:2(CO3)2 ====== CuO + 2CO2↑ + H2O
网址:http://m.1010jiajiao.com/timu_id_233339[举报]
 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:Ⅰ.废铜屑制硝酸铜
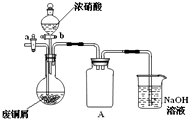
如图(夹持仪器已省略),将浓硝酸缓慢加到废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液.
Ⅱ.碱式碳酸铜的制备
①向大试管中加入碳酸钠溶液和硝酸铜溶液
②水浴加热至70℃左右
③用0.4mol/L的NaOH 溶液调节pH至8.5,振荡、静置、过滤
④用热水洗涤,烘干,得到碱式碳酸铜产品
回答:
(1)浓硝酸与铜反应的离子方程式
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
.(2)装置A的作用是
防止倒吸
防止倒吸
.(3)已知:NO+NO2+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO3+NaNO2+H2O,NO不能单独与NaOH溶液反应,实验结束时,如何操作才能使装置中的有毒气体被NaOH溶液充分吸收?
关闭活塞b,打开活塞a,通入一段时间空气
关闭活塞b,打开活塞a,通入一段时间空气
.(4)步骤④中洗涤的目的是
洗去碱式碳酸铜表面吸附的Na+和NO3-
洗去碱式碳酸铜表面吸附的Na+和NO3-
.(5)步骤③过滤后的滤液中可能含有CO32-,检验CO32- 的方法是
取少量滤液于试管中,加入稀盐酸,将产生的气体通入澄清石灰水,溶液变浑浊,说明有CO32-
取少量滤液于试管中,加入稀盐酸,将产生的气体通入澄清石灰水,溶液变浑浊,说明有CO32-
.(6)若实验得到2.36g 样品(只含CuO 杂质),取此样品加热至分解完全后,得到1.74g 固体,此样品中碱式碳酸铜的质量分数是
0.94或94%
0.94或94%
. 铁、铜和铝是人类生活中常用的金属.
铁、铜和铝是人类生活中常用的金属.(1)地壳中含量最多的金属元素是
铝
铝
.(2)用铜、铝做导线,利用了它们的
导电
导电
性.(3)铁锅易生锈,铁生锈的条件是
潮湿空气
潮湿空气
.(4)铜器表面会生成铜锈,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],该物质含有
4
4
种元素,从它的化学式可推知,铜生锈的过程除了与氧气和水有关外,还与空气中的二氧化碳(或CO2)
二氧化碳(或CO2)
有关.(5)除去铜器表面的铜锈时,加入过量的稀硫酸,生成二氧化碳,同时得到蓝色溶液.若再向上述蓝色溶液中加入足量的铁粉,铁粉与蓝色溶液发生反应的化学方程式为
Fe+CuSO4═FeSO4+Cu、Fe+H2SO4═FeSO4+H2↑
Fe+CuSO4═FeSO4+Cu、Fe+H2SO4═FeSO4+H2↑
.下列10种物质:①水 ②空气 ③铁 ④二氧化碳 ⑤硫酸 ⑥熟石灰[Ca(OH)2]⑦胆矾(CuSO4?5H2O) ⑧NaOH溶液 ⑨碱式碳酸铜[Cu2(OH)2CO3]⑩硫酸氢钠(NaHSO4)
(1)属于混合物的是 .
(2)属于氧化物的是 .
(3)属于碱的是 .
(4)属于酸的是 .
(5)属于盐的是 .(以上空格填物质的序号)
查看习题详情和答案>>
(1)属于混合物的是
(2)属于氧化物的是
(3)属于碱的是
(4)属于酸的是
(5)属于盐的是