网址:http://m.1010jiajiao.com/timu_id_232185[举报]
1
2
3
4
5
6
7
8
9
10
B
D
D
C
A
C
A
A
B
C
11
12
13
14
15
16
17
18
19
20
A
B
AD
B
B
CD
D
C
D
B
21.(4分)BCD
22.(5分)④⑥①③
23、(10分)(1)右(2分),左手拿药匙,右手轻拍左手的手腕,让药匙中的药品轻轻洒落,直到加足药品(3分)。
(2)砝码放在左边,烧杯放在右边(2分),
24.(9分)⑴abcd (3分) (2) ①(3分)2P(s)+3Cl2(g)=2PCl3(g) △H=-612kJ/mol
②(3分)PCl5(g)=PCl3(g)+Cl2(g) △H=+93kJ/mol
25.(12分)⑴Ag+ (2分)
⑵Al3+ (2分) AIO2― + 2H2O + CO2 = Al(OH)3↓+ HCO3- (2分)
⑶NO3- (2分)
⑷不能 (2分) H+和NO3-能把 Fe2+ 氧化为Fe3+ (2分)
26.(14分)(1)C F G (2分)
(2)6Fe2+ + ClO3― + 6 H+ = 6Fe3+ + Cl― + 3H2O (4分),
不影响(2分)
(3)坩埚(2分)
 (4)
(4)
 ×2×
×2× g×100% (4分)
g×100% (4分)
27.(14分)
(1)使Ca2+、Al3+、Fe3+浸出(或使Ca2+、Al3+、Fe3+溶解)(3分)
(2)Ca2++(NH4)
(3)Fe(OH)3、Al(OH)3(各1分,共2分)
(4)Fe3++3SCN― Fe(SCN)3(写成其它正确的络合离子形式给分,2分)
Fe(SCN)3(写成其它正确的络合离子形式给分,2分)
(5)使Fe3+转化为Fe(OH)3沉淀(2分);
⑹检验Al3+(或铝元素)存在 (2分)。
28.(12分) ⑴将含氰化合物全部转化为CN -(2分)
⑵完全吸收HCN,防止气体放空(2分)
⑶防止倒吸(2分)
⑷偏高 (2分)
⑸109.2(4分)
下列溶液中,有关离子一定能大量共存的是
- A.能使石蕊呈红色的溶液中:Na+、S2-、Cl-、NO3-
- B.能使甲基橙呈红色的溶液中:K+、SO32-、SO42-、ClO-
- C.能使pH试纸变兰色的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+
- D.无色溶液中:K+、Cl-、NO3-、SO42-
在下列溶液中,各组离子一定能够大量共存的是
- A.常温下在酸度AG=lg〔c(H+)/c(OH-)〕=10的溶液中:Fe2+、K+、NO3-、SO42-
- B.能溶解NH4HCO3固体产生气泡的溶液中:AlO2-、HCO3-、Ba2+、NO3-
- C.使甲基橙变红的溶液中:NH4+ 、Na+、SO42-、Cl-
- D.能使淀粉碘化钾试纸显蓝色的溶液:K+、NH4+ 、SO42-、S2-
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定:①用 式滴定管盛装c mol/L盐酸标准液。如图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入③表空格中,此时滴定管中液体的体积 mL。
②下表是4种常见指示剂的变色范围: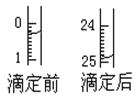
| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0—8.0 | 3.1—4.4 | 4.4—6.2 | 8.2—10.0 |
该实验应选用 作指示剂;
③有关数据记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | | | |
| 3 | V | 6.00 | 31.35 | 25.35 |
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)c = 。
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
A.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果 ;
B.读数时,若滴定前仰视,滴定后俯视,则会使测定结果 ;
C.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果 ;
D.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果 。 查看习题详情和答案>>