摘要::
网址:http://m.1010jiajiao.com/timu_id_218998[举报]
 Ⅰ:反应C(s)+H2O(g)?CO(g)+H2(g)在一容积可变的密闭容器中进行,试回答:
Ⅰ:反应C(s)+H2O(g)?CO(g)+H2(g)在一容积可变的密闭容器中进行,试回答:①增加C的量,其正反应速率的变化是
不变
不变
(填增大、不变、减小,以下相同)②将容器的体积缩小一半,其正反应速率
增大
增大
,逆反应速率增大
增大
.③保持体积不变,充入N2使体系压强增大,其正反应速率
不变
不变
,逆反应速率不变
不变
.④保持压强不变,充入N2使容器的体积增大,其正反应速率
减小
减小
,逆反应速率减小
减小
.Ⅱ:)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.
(1)图中所示反应是
放热
放热
(填“吸热”或“放热”)反应,该反应需要
需要
(填“需要”或“不需要”)加热,该反应的△H=E2-E1
E2-E1
(用含E1、E2的代数式表示).(2)已知热化学方程式:H2(g)+
| 1 | 2 |
409.0KJ/mol
409.0KJ/mol
. Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答:
Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答:(1)该反应的反应物是
A
A
.(2)反应物的转化率是
40%
40%
.(3)该反应的化学方程式为
2A?B+3C
2A?B+3C
.Ⅱ:(7分)在体积为2L的恒容密闭容器中存在以下反应:
CH3OH(g)+H2O(g)?CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
(1)判断该可逆反应达到平衡状态的依据是(填序号)
CD
CD
.A.v正(CH3OH)=v正(CO2) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CH3OH、H2O、CO2、H2的浓度都不再发生变化
(2)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向逆反应方向移动的是
BCF
BCF
(填序号).A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出水蒸气.
Ⅰ:用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如图1所示,分析判断:
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
Ⅱ:某温度时,在2L密闭容器中X、Y、Z三种物质随时间的变化关系曲线如图2所示.
(1)由图2中的数据分析,该反应的化学方程式为
(2)反应开始至2min时 Z的平均反应速率为
(3)5min后Z的生成速率比5min后Z的消耗速率
查看习题详情和答案>>

(1)实验过程如图1所示,分析判断:
E-F
E-F
段化学反应速率最快,E-F
E-F
段收集的二氧化碳气体最多.(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
AC
AC
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
Ⅱ:某温度时,在2L密闭容器中X、Y、Z三种物质随时间的变化关系曲线如图2所示.
(1)由图2中的数据分析,该反应的化学方程式为
3X(g)+Y(g)?2Z(g)
3X(g)+Y(g)?2Z(g)
(2)反应开始至2min时 Z的平均反应速率为
0.05mol/Lmin
0.05mol/Lmin
;(3)5min后Z的生成速率比5min后Z的消耗速率
相等
相等
(大、小、相等).Ⅰ:某些化学反应可表示为:A+B→C+D+H2O,请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为
(2)若A为淡黄色固体,C为无色的气体,则该反应的离子方程式为
(3)若A、C、D均是铁的化合物,B是稀硫酸,则A与B反应的化学方程式为
Ⅱ:某些化学反应可表示为:A+B+H2O→C+D.请回答下列问题:
(1)若A为非金属单质,C为非金属单质,写出符合要求的化学反应方程式
(2)若A为金属单质,C为非金属单质,写出符合要求的离子方程式
查看习题详情和答案>>
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为
Cl2+2OH-=Cl-+ClO-+H2O(或3Cl2+6OH-
5Cl-+ClO3-+3H2O)
| ||
Cl2+2OH-=Cl-+ClO-+H2O(或3Cl2+6OH-
5Cl-+ClO3-+3H2O)
.
| ||
(2)若A为淡黄色固体,C为无色的气体,则该反应的离子方程式为
2Na2O2+4H+═O2↑+4Na++2H2O
2Na2O2+4H+═O2↑+4Na++2H2O
.(3)若A、C、D均是铁的化合物,B是稀硫酸,则A与B反应的化学方程式为
Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
.Ⅱ:某些化学反应可表示为:A+B+H2O→C+D.请回答下列问题:
(1)若A为非金属单质,C为非金属单质,写出符合要求的化学反应方程式
Si+2NaOH+H2O=Na2SiO3+2H2↑
Si+2NaOH+H2O=Na2SiO3+2H2↑
(2)若A为金属单质,C为非金属单质,写出符合要求的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.Ⅰ:碱存在下,卤代烃与醇反应生成醚(R-O-R′):R-X+R′OH
R-O-R′+HX化合物A经下列四步反应可得到常用溶剂四氢 呋喃,反应框图如图一所示:
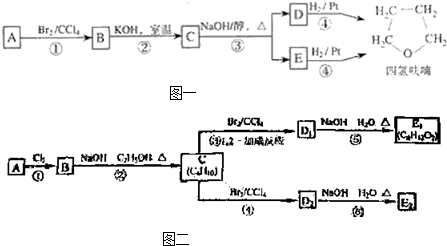
请回答下列问题:
(1)1mol A和1mol H2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%,则Y的分子式为
(2)第①②步反应类型分别为①
(3)化合物B具有的化学性质(填写字母代号)是
a.可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
c.可发生酯化反应 d.催化条件下可发生加聚反应
(4)写出C、D和E的结构简式:C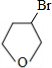
 、D
、D
 、E
、E
 .
.
(5)写出化合物C与NaOH水溶液反应的化学方程式: +NaOH
+NaOH
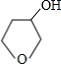 +NaBr
+NaBr +NaOH
+NaOH
 +NaBr.
+NaBr.
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
Ⅱ:某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢.
(1)A的结构简式为
(2)A中碳原子是否都处于同一平面?
(3)在图二中,D1、D2互为同分异构体,E1、E2互为同分异构体.
反应②的化学方程式为
查看习题详情和答案>>
| KOH/室温 |

请回答下列问题:
(1)1mol A和1mol H2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%,则Y的分子式为
C4H10O
C4H10O
.A分子中所含官能团的名称是羟基、碳碳双健
羟基、碳碳双健
.A的结构简式为CH2=CHCH2CH2OH
CH2=CHCH2CH2OH
.(2)第①②步反应类型分别为①
加成反应
加成反应
,②取代反应
取代反应
.(3)化合物B具有的化学性质(填写字母代号)是
abc
abc
.a.可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
c.可发生酯化反应 d.催化条件下可发生加聚反应
(4)写出C、D和E的结构简式:C






(5)写出化合物C与NaOH水溶液反应的化学方程式:
 +NaOH
+NaOH| 水 |
 +NaBr
+NaBr +NaOH
+NaOH| 水 |
 +NaBr
+NaBr(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
CH2=CHOCH2CH3、CH2=CHCH2OCH3、CH3CH=CHOCH3、CH2=C(CH3)OCH3
CH2=CHOCH2CH3、CH2=CHCH2OCH3、CH3CH=CHOCH3、CH2=C(CH3)OCH3
.Ⅱ:某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢.
(1)A的结构简式为
(CH3)2C=C(CH3)2
(CH3)2C=C(CH3)2
;(2)A中碳原子是否都处于同一平面?
是
是
(填“是”或“不是”);(3)在图二中,D1、D2互为同分异构体,E1、E2互为同分异构体.
反应②的化学方程式为
(CH3)2C(Cl)C(Cl)(CH3)2+2NaOH
CH2=C(CH3)-C(CH3)=CH2+2NaCl+2H2O
| 醇 |
| △ |
(CH3)2C(Cl)C(Cl)(CH3)2+2NaOH
CH2=C(CH3)-C(CH3)=CH2+2NaCl+2H2O
;C 的化学名称是| 醇 |
| △ |
2,3-二甲基-1,3-丁二烯
2,3-二甲基-1,3-丁二烯
;E2的结构简式是HOCH2C(CH3)=C(CH3)CH2OH
HOCH2C(CH3)=C(CH3)CH2OH
;④、⑥的反应类型依次是加成反应
加成反应
;取代反应
取代反应
.