摘要:(2)E:H2N― ―CHCOOC2H5,F:CH2CCH2-NH― ―CHCOOC2H5
网址:http://m.1010jiajiao.com/timu_id_217192[举报]
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示.请回答下列问题:
(1)B、C、D元素的非金属性由大到小的顺序为
(2)E的氢化物与其最高价氧化物对应水化物的钾盐共热能发生反应,生成一种气体单质.反应的化学方程式为
(3)C有多种氧化物,其中甲的相对分子质量最小,在一定条件下2L甲气体与0.5L氧气相混合,若该气体混合物被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是
(4)在298K下,A、B的单质各1mol 完全燃烧,分别放出热量aKJ和bKJ,又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来.若此置换反应生成3mol B的单质,则该反应在298K下的△H
(5)要证明与D同主族且相邻的元素的非金属性与E的非金属性强弱,正确、合理的实验操作及现象是
查看习题详情和答案>>
| B | C | D | ||
| A | E |
O>N>C
O>N>C
;(填元素符号)(2)E的氢化物与其最高价氧化物对应水化物的钾盐共热能发生反应,生成一种气体单质.反应的化学方程式为
8HCl+KClO4
KCl+4Cl2↑+4H2O
| ||
8HCl+KClO4
KCl+4Cl2↑+4H2O
;
| ||
(3)C有多种氧化物,其中甲的相对分子质量最小,在一定条件下2L甲气体与0.5L氧气相混合,若该气体混合物被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是
NaNO2
NaNO2
;(4)在298K下,A、B的单质各1mol 完全燃烧,分别放出热量aKJ和bKJ,又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来.若此置换反应生成3mol B的单质,则该反应在298K下的△H
-(4a-3b)KJ/mol
-(4a-3b)KJ/mol
(注:题中所设单质的为稳定单质).(5)要证明与D同主族且相邻的元素的非金属性与E的非金属性强弱,正确、合理的实验操作及现象是
将氯气(或氯水)滴入硫化钠溶液中,有淡黄色沉淀生成
将氯气(或氯水)滴入硫化钠溶液中,有淡黄色沉淀生成
. 某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.
某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.(1)A为电源的
负极
负极
极;(2)E的电极反应式为:
2H++2e-=H2↑
2H++2e-=H2↑
;(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
2:1:2:2
2:1:2:2
;(4)在常温下,现用丙装置给铁镀铜,则H电极材料应该是
铜
铜
,当丙中铁表面析出铜的3.2g时,乙中溶液的PH值为13
13
(假设溶液体积为1L);(5)在电解一段时间后在甲中加入适量
CuO(若考虑到水开始电解Cu(OH)2也可以)
CuO(若考虑到水开始电解Cu(OH)2也可以)
可以使溶液恢复到原来的浓度.[化学--选修3物质结构与性质]A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中A含有3个能级,且每个能 级所含的电子数相同;C的最外层有6个运动状态不同的电子;D是短周期元素中电负性最 小的元素;E的最高价氧化物的水化物酸性最强;F除最外层原子轨道处于半充满状态,其余 能层均充满电子.G元素与D元素同主族,且相差3个周期.
(1)元素A、B、C的第一电离能由小到大的是 用元素符号表示).
(2)E的最高价含氧酸中E的杂化方式为 .
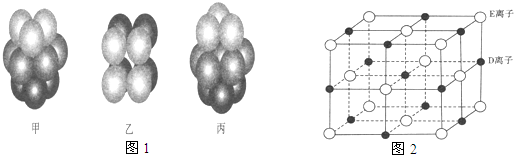
(3)F原子的外围电子排布式为 ,F的晶体中原子的堆积方式是如图1中的 (填写“甲”、“乙”或“丙”).
(4)DE,GE两种晶体,都属于离子晶体,但配位数不同,其原因是
(5)已知DE晶体的晶胞如图2所示若将DE晶胞中的所有E离子去掉,并将D离子全部换为A原子,再在其中的4个“小 立方体”中心各放置一个A原子,且这4个“小立方体”不相邻.位于“小立方体”中的A原 子与最近的4个A原子以单键相连,由此表示A的一种晶体的晶胞(已知A-A键的键长 为a cm,NA表示阿伏加德罗常数),则该晶胞中含有 个A原子,该晶体的密度是 g?cm-3.
查看习题详情和答案>>

(1)元素A、B、C的第一电离能由小到大的是
(2)E的最高价含氧酸中E的杂化方式为
(3)F原子的外围电子排布式为
(4)DE,GE两种晶体,都属于离子晶体,但配位数不同,其原因是
(5)已知DE晶体的晶胞如图2所示若将DE晶胞中的所有E离子去掉,并将D离子全部换为A原子,再在其中的4个“小 立方体”中心各放置一个A原子,且这4个“小立方体”不相邻.位于“小立方体”中的A原 子与最近的4个A原子以单键相连,由此表示A的一种晶体的晶胞(已知A-A键的键长 为a cm,NA表示阿伏加德罗常数),则该晶胞中含有
现有A、B、C、D、E五种短周期元素,其原子序数依次增大.A、C的基态原子电子排布中未成对电子数与其周期数相等,且A的最外层电子数是次外层电子数的2倍.D的阳离子、C的阴离子均与氖原子的电子层结构相同,且D的单质与C的单质反应能生成DC和D2C2两种化合物.E所在周期序数比所在主族序数大l.
(1)2011年是国际化学年,其中一项重要活动是纪念居里夫人获诺贝尔化学奖100周年.居里夫妇发现了放射I生镭(Ra)和钋(Po)元素,其中E与镭同主族,镭位于 族.
(2)E的基态原子的核外电子排布式是 ,A、B、C三种元素中第一电离能最大的是 ,B、C、D的原子半径由小到大的顺序为 (均用元素符号表示).
(3)D2C2与AC2反应的化学方程式为 ,请写出该反应的一种用途 .
(4)B与氢元素形成最简单的气态氢化物的空间构型为 ,其中共价键类型为 (填极性键或非极性键).已知B=B键能为946kJ?mol-1,H-H键能为436kJ?mol-1,B-H键能为391kJ?mol-1,则B2和H2反应的热化学方程式为 .
查看习题详情和答案>>
(1)2011年是国际化学年,其中一项重要活动是纪念居里夫人获诺贝尔化学奖100周年.居里夫妇发现了放射I生镭(Ra)和钋(Po)元素,其中E与镭同主族,镭位于
(2)E的基态原子的核外电子排布式是
(3)D2C2与AC2反应的化学方程式为
(4)B与氢元素形成最简单的气态氢化物的空间构型为
I.硫在空气燃烧生成A,A溶于水得B,B与I2反应得C和D,C与Na2S反应得到含硫化合物E,据此回答下列问题:
(1)写出各物质的分子式:B
(2)E与A、B、C中某种物质反应的方程式
II.加热H2C2O4?2H2O,释放出气体通入澄清石灰水,出现浑浊.
(1)H2C2O4?2H2O热分解反应方程式为
(2)由上可知,Na2C2O4热分解反应方程式为
查看习题详情和答案>>
(1)写出各物质的分子式:B
H2SO3
H2SO3
,DHI
HI
.(2)E与A、B、C中某种物质反应的方程式
2H2S+SO2
3S+2H2O
| ||
2H2S+SO2
3S+2H2O
.
| ||
II.加热H2C2O4?2H2O,释放出气体通入澄清石灰水,出现浑浊.
(1)H2C2O4?2H2O热分解反应方程式为
H2C2O4?2H2O
CO↑+CO2↑+3H2O
| ||
H2C2O4?2H2O
CO↑+CO2↑+3H2O
.
| ||
(2)由上可知,Na2C2O4热分解反应方程式为
Na2C2O4
Na2CO3+CO↑
| ||
Na2C2O4
Na2CO3+CO↑
.
| ||