网址:http://m.1010jiajiao.com/timu_id_214509[举报]
1g氢气燃烧生成液态水,放出142.9KJ热量,下列表示该反应的热化学方程式正确的是
[ ]
A.H2(g)+![]() O2(g)
O2(g)![]() H2O(l) △H=-285.8kJ/mol
H2O(l) △H=-285.8kJ/mol
B.2H2(g)+O2(g)![]() 2H2O(l) △H=-142.9kJ/mol
2H2O(l) △H=-142.9kJ/mol
C.2H2+O2![]() H2O △H=-571.6kJ/mol
H2O △H=-571.6kJ/mol
D.2H2(g)+O2(g)![]() 2H2O(l) △H=+571.6kJ/mol
2H2O(l) △H=+571.6kJ/mol
1g氢气燃烧生成液态水,放出142.9kJ热量,下列表示该反应的热化学方程式正确的是
[ ]
A.2H2(g)+O2(g)=2H2O(l);ΔH=-142.9kJ·mol-1
B.H2(g)+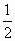 O2(g)=H2O(l);ΔH=-285.8kJ·mol-1
O2(g)=H2O(l);ΔH=-285.8kJ·mol-1
C.2H2(g)+O2=2H2O(l);ΔH=-571.6kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l);ΔH=+571.6kJ·mol-1
查看习题详情和答案>>1g氢气燃烧生成液态水放出142.9kJ热量,下列表示该反应的热化学方程式正确的是
A. 2H2(g)+O2(g)=2H2O(l) △H=-142.9kJ/mol
B. H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol
C. 2H2(g)+O2=2H2O(l) △H=-571.6kJ/mol
D. 2H2(g)+O2(g)=2H2O(l) △H=+571.6kJ/mol
查看习题详情和答案>>(1)实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为
A.2H2(g)+O2(g)=2H2O(l);△H=-142.9kJ?mol-1
B.H2(g)+
| 1 |
| 2 |
C.2H2+O2=2H2O(l);△H=-571.6kJ?mol-1
D.H2(g)+
| 1 |
| 2 |
(2)某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤
①CaBr2+H2O
| ||
②2HBr+Hg
| ||
③HgBr2+
| ||
④2HgO
| ||
⑤2H2+O2
| ||
请你根据“原子经济”的思想完成上述步骤③的化学方程式:
(3)利用核能把水分解制氢气,是目前正在研究的课题.如图1是其中的一种流程,其中用了过量的碘.
完成下列反应的化学方程式:反应①
(4)目前有科学家在一定条件下利用水煤气(CO+H2)合成甲醇:
CO(g)+2H2(g)
| CuO/ZnO |
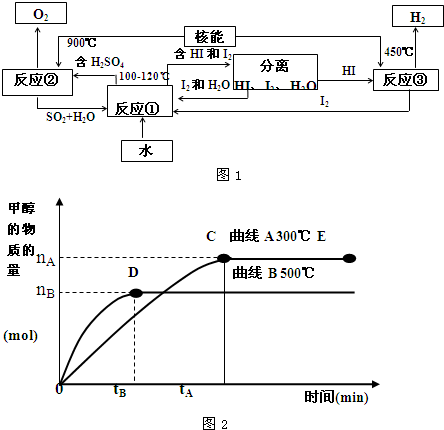
①合成甲醇反应,其反应热△H
②其它条件不变,对处于E点的体系体积压缩到原来的
| 1 |
| 2 |
| c(CH3OH) |
| c(CO) |
③据研究,合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)
(15分)科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是 。(选填字母)
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |

(3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量写出其完全燃烧的热化学方程式: 。
(4)利用氢气和CO合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)
 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1② 2CH3OH(g)
 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1③ CO(g) + H2O(g)
 CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1总反应:3H2(g) + 3CO(g)
 CH3OCH3(g) + CO2 (g)的ΔH=
CH3OCH3(g) + CO2 (g)的ΔH= (5)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:

①氢氧燃料电池中,正极的电极反应式为 。
②上图装置中,某一铜电极的质量减轻3.2g,则 a 极上消耗的O2在标准状况下的体积为
L。
(6)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。则正极电极方程式 。 查看习题详情和答案>>