摘要:2+O2+2H2O 4Fe(OH)3 2Al+Fe2O3 2Fe+Al2O3
网址:http://m.1010jiajiao.com/timu_id_209232[举报]
下列反应为吸热反应且能自发进行的是
[ ]
A. 4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)
B. NH4HCO3(s)+CH3 COOH( aq) =CH3 COONH4( aq)+ CO2(g)+H2O(l)
C. 2H2(g)+O2(g)=2H2O(l)
D. 2Al(s)+Fe2O3(s)=Al2O3(s)+2Fe(s)
查看习题详情和答案>>
B. NH4HCO3(s)+CH3 COOH( aq) =CH3 COONH4( aq)+ CO2(g)+H2O(l)
C. 2H2(g)+O2(g)=2H2O(l)
D. 2Al(s)+Fe2O3(s)=Al2O3(s)+2Fe(s)
如图所示:①~⑩分别代表有关反应中的一种物质,它们均为常见物质.已知①~⑤和⑥~⑩中分别含有同一种元素.试回答下列问题:
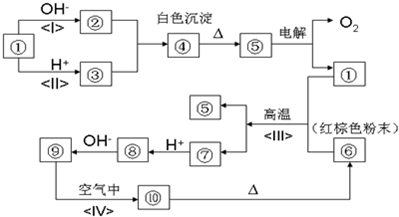
(1)写出指定物质的化学式:④
(2)写出反应(Ⅲ)的化学方程式
(3)写出反应(Ⅰ)的离子方程式
(4)反应(Ⅳ)的主要实验现象是
查看习题详情和答案>>

(1)写出指定物质的化学式:④
Al(OH)3
Al(OH)3
;⑥Fe2O3
Fe2O3
(2)写出反应(Ⅲ)的化学方程式
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
指出该反应的重要用途之一:
| ||
焊接钢轨
焊接钢轨
(3)写出反应(Ⅰ)的离子方程式
2Al+2OH-+2H2O═AlO2-+3H2↑或2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑
2Al+2OH-+2H2O═AlO2-+3H2↑或2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑
(4)反应(Ⅳ)的主要实验现象是
白色沉淀迅速变成灰绿色,最终变成红褐色
白色沉淀迅速变成灰绿色,最终变成红褐色
该反应的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3
4Fe(OH)2+O2+2H2O═4Fe(OH)3
.请根据如下流程和提示回答问题.

提示:①2Cu+
Cu+Cu2+;②AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
(1)滤液A中铁元素的存在形式为
(2)金属E与固体F发生的某一反应可用于焊接钢轨.
①由滤液C生成金属E至少经过
②用于焊接钢轨的化学反应方程式为
(3)固体混合物D在空气中灼烧时发生的氧化还原反应的化学方程式为
查看习题详情和答案>>

提示:①2Cu+
| ||
(1)滤液A中铁元素的存在形式为
Fe2+
Fe2+
(填写离子符号),原因是Cu+2Fe3+=Cu2++2 Fe2+
Cu+2Fe3+=Cu2++2 Fe2+
(书写相应化学方程式即可),检验试剂是KSCN溶液和新制氯水
KSCN溶液和新制氯水
.(2)金属E与固体F发生的某一反应可用于焊接钢轨.
①由滤液C生成金属E至少经过
3
3
步反应,其中属于分解反应的有2
2
个.②用于焊接钢轨的化学反应方程式为
2Al+Fe2O3
Al2O3+2Fe
| ||
2Al+Fe2O3
Al2O3+2Fe
.
| ||
(3)固体混合物D在空气中灼烧时发生的氧化还原反应的化学方程式为
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(2010?抚顺一模)以下框图中A~M是中学化学常见的物质,其中A、E是金属,F和J为气体单质,其余均为化合物或其溶液,C为淡黄色固体,D为红棕色粉末,M为红褐色固体.

请回答下列问题:
(1)B的化学式
(2)19.5gC与足量的水反应转移电子的物质的量为
(3)若将H溶液加热蒸干、灼烧,最终得到的固体物质的化学式
(4)写出①反应的离子方程式
(5)写出②、③反应的化学方程式②
查看习题详情和答案>>

请回答下列问题:
(1)B的化学式
Al2O3
Al2O3
;(2)19.5gC与足量的水反应转移电子的物质的量为
0.25
0.25
mol;(3)若将H溶液加热蒸干、灼烧,最终得到的固体物质的化学式
Fe2O3
Fe2O3
.(4)写出①反应的离子方程式
2Al+2OH-+2H2O=AlO2-+3H2↑
2Al+2OH-+2H2O=AlO2-+3H2↑
.(5)写出②、③反应的化学方程式②
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
,③Fe2O3+2Al
2Fe+Al2O3
| ||
Fe2O3+2Al
2Fe+Al2O3
.
| ||