摘要:22.Al2O3 离子键.非极性键 (2)Fe2O3
网址:http://m.1010jiajiao.com/timu_id_209230[举报]
以下框图中A→M是中学化学中常见的物质,其中A、E是金属,F和J为气体单质,其余均为化合物或其溶液,C为淡黄色固体,D为红棕色粉末,M为红褐色固体.
请回答下列问题:

(1)C的电子式为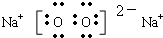
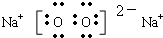 ,C物质中所含化学键类型
,C物质中所含化学键类型
(2)反应①的离子方程式是:
(3)写出B与G溶液反应的离子方程式
(4)在I溶液中通入过量CO2反应的化学方程式
查看习题详情和答案>>
请回答下列问题:

(1)C的电子式为
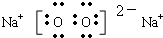
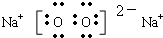
离子键、非极性共价键
离子键、非极性共价键
.(2)反应①的离子方程式是:
2Al+2H2O+2OH-=2AlO2-+3H2↑.
2Al+2H2O+2OH-=2AlO2-+3H2↑.
.(3)写出B与G溶液反应的离子方程式
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.(4)在I溶液中通入过量CO2反应的化学方程式
2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓
2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓
.现有六种元素A、B、C、D、E均为周期表中前18号元素,且原子序数依次增大.已知A和B是形成化合物种类最多的两种元素;B元素和C元素通常形成电子数为14或22的化合物.D元素的原子半径是短周期主族元素中最大的;E元素是地壳中含量最高的金属.请回答以下问题:
(1)请画出D的离子结构示意图
 ;由C、A两种元素形成的18电子化合物的电子式为
;由C、A两种元素形成的18电子化合物的电子式为
 ;
;
(2)E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式:
(3)由以上五种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有
查看习题详情和答案>>
(1)请画出D的离子结构示意图




(2)E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式:
Al2O3+2OH-=2AlO-2+H2O
Al2O3+2OH-=2AlO-2+H2O
;(3)由以上五种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有
Na2O2
Na2O2
(填化学式);它的主要用途是供氧剂、漂白剂
供氧剂、漂白剂
,它与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.