网址:http://m.1010jiajiao.com/timu_id_204226[举报]

(1)写出该反应的化学方程式:__________________。该氧化还原反应的还原剂是____,氧化剂是____。
(2)实验前必须对整套装置进行气密性检查,操作方法是______________。
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_____________;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_________。
(4)酒精灯和酒精喷灯点燃的顺序是_____________,为什么?__________________。
(5)干燥管中盛装的物质是________,作用是_________。
(6)试管中收集的气体是______________。如果要在A处的玻璃管处点燃该气体,则必须对该气体进行_________,方法是______________,这一操作的目的是______________。
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。
图中:①空气②某溶液③纯碱④某溶液⑤碱石灰(注:碱石灰既能吸收CO2,又能吸收H2O)
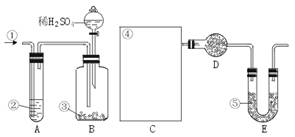 其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是____________________ 。装置A中盛装的液体“2”应选用________________,装置A的作用是________________,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)________________。
(2)在空白格内画出装置C及试剂④是__________ ;装置C的作用是________________;如果撤去装置C,则会导致测定结果________________(填“偏大”“偏小”或“不变”)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________________(用m1、m2、n表示)
(4)装置E的作用是________________________。
查看习题详情和答案>>纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。图中:①空气②某溶液③纯碱④某溶液⑤碱石灰(注:碱石灰既能吸收CO2,又能吸收H2O)
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。根据上述实验回答下列问题:

(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是____________________ 。装置A中盛装的液体“2”应选用________________,
(2)在空白格内画出装置C及试剂④是______ ____ ;如果撤去装置C,则会导致测定结果________________(填“偏大”“偏小”或“不变”)
(3)装置E的作用是________________________
(4)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________________(用m1、m2、n表示)
查看习题详情和答案>>纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数.图中:
①空气
②某溶液
③纯碱
④某溶液
⑤碱石灰
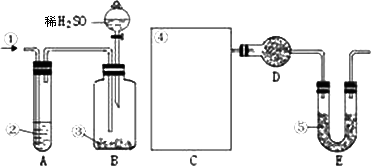
其实验步骤是:
a.按如图所示,组装好实验仪器,并检查其气密性.
b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g).
c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内.
d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“①”处缓慢鼓入空气,直到B容器中不再产生气体为止.
e.准确称量干燥管D的总质量(设为m2 g).
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是________.装置A中盛装的液体“②”应选用________,装置A的作用是________,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)________.
(2)在空白格内画出装置C及试剂④是________;装置C的作用是________;如果撤去装置C,则会导致测定结果________(填“偏大”、“偏小”或“不变”)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________(用m1、m2、n表示)
(4)装置E的作用是________.
化学实验兴趣小组在实验室 进行氢气在氯气中的燃烧实验。
设计如下图所示装置I制备和收焦干燥纯净的氯气以备后续实验;

烧瓶中发生反应的离子方程式为 ;
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;
在右图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CaSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。

①检查制取氢气装置气密性的操作方法是
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示); ;B组同学向集气瓶中注入适量水,用力振荡后,向中满入少量Na2SO3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。[已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O],同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:
①
②
查看习题详情和答案>>