摘要:⑷ S2-+ Na2O2 + 2H2O == S +4OH-+2Na+ 19 ?8分?①c. 浓硫酸吸水 d. 称量碱石灰吸收二氧化碳并称量 a .b 和c分别为 3 1 3 ② n?Mg?┱n?Si?= 2:1
网址:http://m.1010jiajiao.com/timu_id_204177[举报]
A、B、C、D、E均为短周期元素,且原子序数逐渐增大.A、D最外层电子数相等且能形成离子化合物,A与B的质子数之和等于C的质子数,A+与 C2-的核外电子数之和等于D+离子的核外电子数,B 原子与 D+离子的核外电子数之和等于 E 原子的核外电子数.
(1)B的元素符号为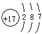
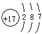 ;由A、C、E三种元素组成的化合物具有漂白性,其电子式为
;由A、C、E三种元素组成的化合物具有漂白性,其电子式为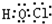
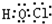 .
.
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
查看习题详情和答案>>
(1)B的元素符号为
N
N
,E的原子结构示意图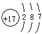
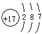
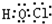
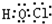
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
.(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
NH4NO3
NH4NO3
,物质乙抑制水的电离HNO3
HNO3
;室温下,若两溶液的pH都为4,则两溶液中水电离的氢离子浓度比为:甲:乙=106
106
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
>
>
7(填“>”“<”“=”),溶液中离子浓度由大到小的顺序为C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C(NH4+)>C(Cl-)>C(OH-)>C(H+)
.(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
H2+2e-+2OH-=2H2O
H2+2e-+2OH-=2H2O
. 某学习小组为测定市售过氧化钠纯度,设计了如下方案:
某学习小组为测定市售过氧化钠纯度,设计了如下方案:实验原理:2Na2O2+2H2O═4NaOH+O2↑(杂质不参与反应)
仪器装置:如图.
实验步骤:
①称取过氧化钠样品2.00g;
②把过氧化钠样品放入气密性良好的气体发生装置锥形瓶中(固体体积忽略不计);
③向过氧化钠样品中滴加水,用量气装置测得气体体积为166.00mL(已换算成标准状况);
④锥形瓶中液体体积为54.00mL;
⑤将锥形瓶内液体全部转移入仪器A中,并定容至250.00mL;
请回答下列问题:
(1)仪器A的名称:
(2)生成气体的体积为
(3)据报导,该反应还会有副反应:Na2O2+2H2O═2NaOH+H202,H2O2生成,会使测定结果
(4)为效正实验结果.该小组补做了如下实验:用滴定管量取20.00mL.A中的液体放入锥形瓶中,用0.010mol/L.的H2SO4酸化的高锰酸钾溶液滴定至终点,用去12.00ml.高锰酸钾溶液.其反应为:(未配平)KMnO4+H2O2+H2SO4→K2SO4+MnSO4+O2+H2O
①滴定时高锰酸钾溶液应装在
②此实验未使用指示剂,如何确定终点:
③由上述实验测定数据,计算该过氧化钠样品纯度(写出计算过程). 查看习题详情和答案>>
已知,0℃时发生反应:Na2O2+2H2O=2NaOH+H2O2,下列化学用语表示正确的是( )
A、H2O2的电子式为 | ||||||
B、O2-、Na的结构示意图都可以用 表示 表示 | ||||||
| C、H2O、NaOH、Na2O2中氧元素的化合价均为-2 | ||||||
D、
|
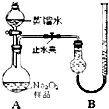 (2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.
(2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.[实验一]取样品0.100g,用如图所示实验装置进行测定.(夹持装置省略)
(1)检查装置A气密性的方法是
夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好;或者关闭分液漏斗活塞,右侧的导管插入水中,用手捂住分液漏斗,看是否有气泡产生,冷却后是否有一段水柱形成
夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好;或者关闭分液漏斗活塞,右侧的导管插入水中,用手捂住分液漏斗,看是否有气泡产生,冷却后是否有一段水柱形成
.(2)若在实验过程中共产生气体11.20mL(已折算成标准状况),则样品中Na2O2的纯度为
78%
78%
.[实验二]样品溶于水后用盐酸滴定
(3)取一定量样品溶于水并稀释至250mL,配制时,所用到的玻璃仪器除了烧杯和玻璃棒外,还需用到
250 mL容量瓶、胶头滴管
250 mL容量瓶、胶头滴管
.(4)取上述所配溶液各25.00mL,用一定浓度的标准盐酸滴定,平行实验记录如下表:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 标准盐酸体积(mL) | 23.00 | 24.98 | 25.00 | 25.02 |
25.00
25.00
mL.若滴定前用上述所配溶液润洗锥形瓶,对实验测定结果产生的影响是偏高
偏高
(填“偏高”、“偏低”或“无影响”).[实验分析]实验结果对比分析
(5)小组同学对比两个实验发现,实验一测得的Na2O2样品的纯度比理论值明显偏小.经过分析,小组同学认为,明显偏差不是由操作失误和装置缺陷引起的,可能是反应原理上的原因.查阅资料发现:Na2O2与水反应产生的H2O2未完全分解.
①写出Na2O2与水生成H2O2的化学方程式
Na2O2+2H2O=2NaOH+H2O2
Na2O2+2H2O=2NaOH+H2O2
.②若将实验一稍加改进,就能使测定结果接近理论值,写出改进方案:
反应前向Na2O2样品中加入少量MnO2
反应前向Na2O2样品中加入少量MnO2
.