摘要:C.硫酸的物质的量浓度为2.5 mol?L-1
网址:http://m.1010jiajiao.com/timu_id_199778[举报]
硫酸钡是唯一的无毒的钡盐,工业上以硫酸钡等为原料通过下列流程反应可以制备锌钡白(BaSO4+ZnS)和过氧化氢.(皓矾为ZnSO4?7H2O)

(1)上述流程中共有7个化学反应,其中有 个属于氧化还原反应.
(2)写出过氧化氢和物质C的电子式: , .
(3)写出F、G的化学式:F 、G .
(4)写出下列化学反应方程式:反应③ .反应⑦ .
(5)取锌钡白固体16.5g溶于100mL 1mol/L的H2SO4 溶液中,放出H2S 气体1008mL(已折算成标准状况)
①不计溶液体积变化,所得溶液中氢硫酸的物质的量浓度为 mol/L;
②加热驱尽溶液中H2S 后,为使锌离子刚好完全沉淀,应加入 1mol/L的NaOH溶液 mL.
查看习题详情和答案>>

(1)上述流程中共有7个化学反应,其中有
(2)写出过氧化氢和物质C的电子式:
(3)写出F、G的化学式:F
(4)写出下列化学反应方程式:反应③
(5)取锌钡白固体16.5g溶于100mL 1mol/L的H2SO4 溶液中,放出H2S 气体1008mL(已折算成标准状况)
①不计溶液体积变化,所得溶液中氢硫酸的物质的量浓度为
②加热驱尽溶液中H2S 后,为使锌离子刚好完全沉淀,应加入 1mol/L的NaOH溶液
硫酸钡是唯一的无毒的钡盐,工业上以硫酸钡等为原料通过下列流程反应可以制备锌钡白(BaSO4+ZnS)和过氧化氢.(皓矾为ZnSO4?7H2O)

(1)上述流程中共有7个化学反应,其中有______个属于氧化还原反应.
(2)写出过氧化氢和物质C的电子式:______,______.
(3)写出F、G的化学式:F______、G______.
(4)写出下列化学反应方程式:反应③______.反应⑦______.
(5)取锌钡白固体16.5g溶于100mL 1mol/L的H2SO4 溶液中,放出H2S 气体1008mL(已折算成标准状况)
①不计溶液体积变化,所得溶液中氢硫酸的物质的量浓度为______mol/L;
②加热驱尽溶液中H2S 后,为使锌离子刚好完全沉淀,应加入 1mol/L的NaOH溶液______mL.
查看习题详情和答案>>
硫酸钡是唯一的无毒的钡盐,工业上以硫酸钡等为原料通过下列流程反应可以制备锌钡白(BaSO4+ZnS)和过氧化氢:(皓矾为ZnSO4·7H2O)

(1)上述流程中共有7个化学反应,其中有____________个属于氧化还原反应。
(2)写出过氧化氢和物质C的电子式:____________________,_______________。
(3)写出F、G的化学式: F_____________、G_________________。
(4)写出下列化学反应方程式:反应③_______________________________。
反应⑦________________________。
(5)取锌钡白固体16.5g溶于100mL 1mol/L的H2SO4溶液中,放出H2S气体1008mL(已折算成标准状况) ①不计溶液体积变化,所得溶液中氢硫酸的物质的量浓度为________mol/L
②加热驱尽溶液中H2S后,为使锌离子完全沉淀,应加入1mol/L的NaOH溶液__________mL。
查看习题详情和答案>>
(2)写出过氧化氢和物质C的电子式:____________________,_______________。
(3)写出F、G的化学式: F_____________、G_________________。
(4)写出下列化学反应方程式:反应③_______________________________。
反应⑦________________________。
(5)取锌钡白固体16.5g溶于100mL 1mol/L的H2SO4溶液中,放出H2S气体1008mL(已折算成标准状况) ①不计溶液体积变化,所得溶液中氢硫酸的物质的量浓度为________mol/L
②加热驱尽溶液中H2S后,为使锌离子完全沉淀,应加入1mol/L的NaOH溶液__________mL。
有浓度均为0.1mol?L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a mol?L-1,b mol?L-1,c mol?L-1,其由大到小顺序为
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n1mol,n2 mol,n3 mol,它们的大小关系为
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为
(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3,其由大到小顺序为
(5)三种溶液溶液分别稀释100倍,稀释后三种溶 液的c(H+)分别为c1、c2和c3,则c1、c2和c3的大小关系为
查看习题详情和答案>>
(1)三种溶液中c(H+) 依次为a mol?L-1,b mol?L-1,c mol?L-1,其由大到小顺序为
b>a>c
b>a>c
.(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n1mol,n2 mol,n3 mol,它们的大小关系为
n 1=n2=n3
n 1=n2=n3
.(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为
V1=2V2=V3
V1=2V2=V3
.(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3,其由大到小顺序为
v2>v1>v3
v2>v1>v3
.(5)三种溶液溶液分别稀释100倍,稀释后三种溶 液的c(H+)分别为c1、c2和c3,则c1、c2和c3的大小关系为
c2>c1>c3
c2>c1>c3
.生物质资源是一种污染小的可再生能源,可由其制得多种化工原料,如甲醛、甲醇和二甲醚等.
(1)甲醛溶液可用于浸制生物标本,这主要是利用了甲醛的何种化学性质 .
(2)由生物质能获得的CO和H2,可以合成多种有机物.当CO和H2以物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是 .
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ/mol.
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得
反应达到平衡时的有关数据如下:
下列说法正确的是 .
A.cl=c2 B.2Q1=Q3 C.KI=K3 D.a2+a3<100%
(4)一定温度和压强下,CO和H2催化合成二甲醚的反应为:
3H2 (g)+3CO (g) CH3OCH3 (g)+CO2(g)
若一体积可变的密闭容器中充入3mol H2、3molCO、l mol CH3OCH3、l mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍.平衡时
n(CH3OCH3)= mol.反应开始时正、逆反应速率的大小:v(正) v(逆)(填‘‘>’’、“<”或“=”),理由是 .
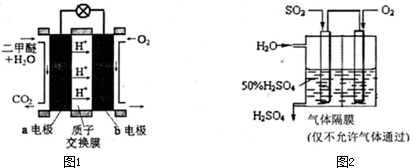
(5)如图1为绿色电源“直接二甲醚燃料电池”的工作原理示意图.b电极是 极,a电极的反应式为 .
(6)利用生物质资源过程中会产生SO2,可利用如图2所示装置,用电化学原理生产硫酸为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为 .
查看习题详情和答案>>
(1)甲醛溶液可用于浸制生物标本,这主要是利用了甲醛的何种化学性质
(2)由生物质能获得的CO和H2,可以合成多种有机物.当CO和H2以物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ/mol.
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得
反应达到平衡时的有关数据如下:
| 1.容器 | 2.甲 | 3.乙 | 4.丙 |
| 5.反应物投入量 | 6.1molCO、2molH2 | 7.l molCH3OH | 8.2molCO、4molH2 |
| 9.CH30H昀浓度(mol/L) | 10.cl | 11.c2 | 12.c3 |
| 13.反应的能量变化 | 14.放出Q1kJ | 15.吸收Q2kJ | 16.放出Q3kJ |
| 17.平衡常数 | 18.Kl | 19.K2 | 20.K3 |
| 21.反应物转化率 | 22.al | 23.a2 | 24.a3 |
A.cl=c2 B.2Q1=Q3 C.KI=K3 D.a2+a3<100%
(4)一定温度和压强下,CO和H2催化合成二甲醚的反应为:
3H2 (g)+3CO (g) CH3OCH3 (g)+CO2(g)
若一体积可变的密闭容器中充入3mol H2、3molCO、l mol CH3OCH3、l mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍.平衡时
n(CH3OCH3)=

(5)如图1为绿色电源“直接二甲醚燃料电池”的工作原理示意图.b电极是
(6)利用生物质资源过程中会产生SO2,可利用如图2所示装置,用电化学原理生产硫酸为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为