摘要:C.10.2g该酸的物质的量为0.6mol D.该酸的相对分子质量为68
网址:http://m.1010jiajiao.com/timu_id_195807[举报]
完全中和5.1g二元酸H2A生成正盐,用去12g NaOH,则关于二元酸的说法正确的是
[ ]
A.该酸的摩尔质量是17g.mol-1
B.该酸中A的相对原子质量是34g.mol-1
C.10. 2g该酸的物质的量是0.3mol
D.该酸一定是强酸
查看习题详情和答案>>
B.该酸中A的相对原子质量是34g.mol-1
C.10. 2g该酸的物质的量是0.3mol
D.该酸一定是强酸
完全中和5.1g二元酸H2A生成正盐,用去12g NaOH,则下列关于该二元酸的说法正确的是()。
A.该酸的摩尔质量是17g?mol-1
B.该酸中A的相对原子质量是34g?mol-1
C.10.2g该酸的物质的量是0.3mol
D.该酸一定是强酸 查看习题详情和答案>>
A.该酸的摩尔质量是17g?mol-1
B.该酸中A的相对原子质量是34g?mol-1
C.10.2g该酸的物质的量是0.3mol
D.该酸一定是强酸 查看习题详情和答案>>
某元素X的相对原子质量为a,它的最高价氧化物的水化物的化学式为HmXOn(m>1)。下列有关叙述正确的是()
- A.该酸的水溶液中c(H+)∶c(XOnm-)=m∶1
- B.该酸的摩尔质量为(m+a+16n)g
- C.100mL该酸溶液,只能中和4gNaOH
- D.若0.1mol×L-1该酸溶液的pH=1,则NamXOn的水溶液的pH>7
(2013?珠海模拟)锌锰废电池可回收锌、锰元素生产硫酸锌及碳酸锰,其中生产工业级碳酸锰工艺如下:
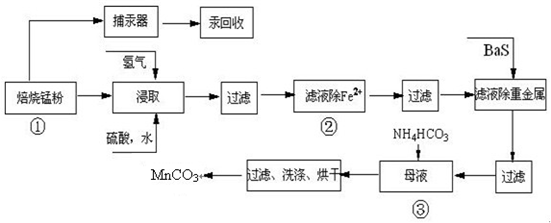
试回答下列问题:
(1)硫酸锌水溶液显酸性,用离子方程式说明
(2)原料锰粉粗品中主要成分为MnO2和碳,焙烧时反应的化学方程式为MnO2+C=MnO+CO↑,该反应的氧化产物是
(3)50-55℃向MnS04的母液中加入足量NH4HC03,反应的化学方程式为:
MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+
(4)已知三种离子沉淀的pH范围为Fe3+:2.7~3.7,Mn2+:8.6~10.1,Fe2+:7.6~9.6.下表是上述过程②中除去Fe2+的模拟操作方法,请完成下表内容:
查看习题详情和答案>>

试回答下列问题:
(1)硫酸锌水溶液显酸性,用离子方程式说明
Zn2++2H2O?Zn(OH)2+2H+
Zn2++2H2O?Zn(OH)2+2H+
.(2)原料锰粉粗品中主要成分为MnO2和碳,焙烧时反应的化学方程式为MnO2+C=MnO+CO↑,该反应的氧化产物是
CO
CO
.(3)50-55℃向MnS04的母液中加入足量NH4HC03,反应的化学方程式为:
MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+
H2O
H2O
+CO2↑
CO2↑
.(4)已知三种离子沉淀的pH范围为Fe3+:2.7~3.7,Mn2+:8.6~10.1,Fe2+:7.6~9.6.下表是上述过程②中除去Fe2+的模拟操作方法,请完成下表内容:
| 实验操作 | 离子方程式 |
| 步骤1:取少量滤液于试管中,加入过量酸化的H2O2溶液,振荡. | 2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe2++H2O2+2H+=2Fe3++2H2O |
| 步骤2:将pH调到 3.7~8.6 3.7~8.6 ,使Fe3+沉淀完全 |
Fe3++3H2O?Fe(OH)3+3H+ |
(2013?武清区三模)X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是生活中最常用的金属,它与L可以形成三种化合物.
请回答下列问题:
(1)M在元素周期表中的位置为
(2)X 分别与Z和L 形成的化合物A和B都含有18e-,A是一种6原子分子,可做火箭发动机的燃料,B是一种常见强氧化剂.已知16g液态A与液态B充分反应生成一种液态10电子分子C和一种气态单质,并放出838kJ热量.写出A与B反应的热化学方程式
(3)已知(YZ)2分子所有的原子都满足8电子,请写出其结构式
(4)YL2的电子式是
 ,其分子的空间构型是
,其分子的空间构型是
(5)M在高温下可以与C反应,写出该反应的化学方程式
某同学将反应得到的黑色粉末全部溶于足量的硫酸溶液中,发现有少量的气泡产生,溶液呈棕黄色,该同学判断溶液中一定同时存在两种M的金属阳离子.若该同学将上述棕黄色溶液1mL加入到2mL A的浓溶液中,预计会看到的实验现象是
查看习题详情和答案>>
请回答下列问题:
(1)M在元素周期表中的位置为
第四周期第VIII族
第四周期第VIII族
(2)X 分别与Z和L 形成的化合物A和B都含有18e-,A是一种6原子分子,可做火箭发动机的燃料,B是一种常见强氧化剂.已知16g液态A与液态B充分反应生成一种液态10电子分子C和一种气态单质,并放出838kJ热量.写出A与B反应的热化学方程式
N2H4(l)+2H2O2(l)=4H2O(l)+N2(g)△H=-1676kJ/mol
N2H4(l)+2H2O2(l)=4H2O(l)+N2(g)△H=-1676kJ/mol
(3)已知(YZ)2分子所有的原子都满足8电子,请写出其结构式
N≡C-C≡N
N≡C-C≡N
;(YZ)2可以与X2化合生成XYZ,其水溶液是一种酸,某浓度该酸的钾盐(KYZ)溶液能使酚酞溶液显红色,请用离子方程式表示原因CN-+H2O=HCN+OH-
CN-+H2O=HCN+OH-
(4)YL2的电子式是


直线型
直线型
(5)M在高温下可以与C反应,写出该反应的化学方程式
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
| ||
某同学将反应得到的黑色粉末全部溶于足量的硫酸溶液中,发现有少量的气泡产生,溶液呈棕黄色,该同学判断溶液中一定同时存在两种M的金属阳离子.若该同学将上述棕黄色溶液1mL加入到2mL A的浓溶液中,预计会看到的实验现象是
有大量气泡出现
有大量气泡出现
.