网址:http://m.1010jiajiao.com/timu_id_189600[举报]

[实验设计]在小烧杯中加入25 mL蒸馏水,加热至沸腾,慢慢滴入1~2 mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,即可得Fe(OH)3胶体。实现现象:烧杯中液体呈红褐色。化学方程式:
FeCl3+3H2OFe(OH)3(胶体)+3HCl
(1)实验中必须要用蒸馏水,而不能用自来水。原因是_________________。
(2)实验操作中,必须选用饱和氯化铁溶液而不能用稀氯化铁溶液。原因是______________________。
(3)往沸水中滴加饱和氯化铁溶液后,可稍微加热煮沸,但不宜 长时间加热。这样操作的原因是______________________。
| ||
(1)判断胶体制备是否成功,可利用胶体的
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化.
①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
(1)该过程的化学方程式为
(2)设计较简单的方法判断胶体已制备成功
(3)向该胶体中逐滴加入4mol/L的盐酸,会出现一系列变化:
a.先出现
|
下列离子方程式与所述事实相符且正确的是 | |
| [ ] | |
A. |
漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO |
B. |
AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
C. |
等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合: Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2O |
D. |
向沸水中滴加 FeCl3饱和溶液制取Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+
|
无机化学反应式
1、2Na+2H2O=2NaOH+H2↑ ★ 2K+2H2O=2KOH+H2↑
2、2Na2O2+2H2O=4NaOH+O2↑ 3、2Na2O2+2CO2=2Na2CO3+O2
4、氢氧化钠和碳酸氢钠在溶液中反应的离子方程式为:
OH- +HCO3- =CO32- +H2O
氯气溶于水(新制氯水中含Cl2.HClO.H2O .H+ .Cl - .ClO - .OH-):
5、Cl2+H2O=HCl+HClO ★ Cl2+2NaOH=NaCl+NaClO+H2O
次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂):
6、2HClO![]() 2HCl+O2↑
2HCl+O2↑
7、Ca(ClO)2+CO2+H2O=CaCO3+2HClO
8、MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
9、2F2+2H2O=4HF+O2 Cl2+H2O=HCl+HClO Br2+H2O=HBr+HBrO
10、2Al+2NaOH+2H2O=2NaAlO2+3H2↑ Al2O3+2NaOH=2NaAlO2+H2O
Al(OH)3+NaOH=NaAlO2+2H2O
11、H2O2的分解: 2H2O2![]() 2H2O+O2↑ *H2S与SO2的反应: 2H2S+SO2=3S+2H2O
2H2O+O2↑ *H2S与SO2的反应: 2H2S+SO2=3S+2H2O
12、2SO2+O2![]() 2SO3
2SO3
13、Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
14、C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
15、SiO2+2C![]() Si+2CO↑
Si+2CO↑
16、![]()
17、N2+O2 ![]() 2NO 2NO+O2=2NO2 3NO2+H2O=2HNO3+NO
2NO 2NO+O2=2NO2 3NO2+H2O=2HNO3+NO
18、4NH3 +5O2 4NO+6H2O
4NO+6H2O
19、用浓盐酸检验氨气(白烟生成): NH3+HCl=NH4Cl
20、(NH4)2SO4+2NaOH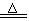 Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O
21、NH4NO3+NaOH=NaNO3+NH3↑+H2O
22、4HNO3![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
23、Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
C+4HNO3(浓)=CO2↑+4NO2↑+2H2O
24、FeCl3+3KSCN![]() 3KCl+Fe(SCN)3
3KCl+Fe(SCN)3
25、盐类水解: CH3COO- +H2O![]() CH3COOH+OH- CO32- +H2O
CH3COOH+OH- CO32- +H2O![]() HCO3-+OH-
HCO3-+OH-
HCO3- +H2O![]() H2CO3+OH- NH4+ +H2O
H2CO3+OH- NH4+ +H2O![]() NH3?H2O+H+
NH3?H2O+H+
Fe3+ +3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
27、铝热反应: 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
4Al+3MnO2![]() 3Mn+2Al2O3
3Mn+2Al2O3
28、2Mg+CO2![]() C+2MgO
C+2MgO
29、Al2(SO4)3+6NH3·¤H2O=2Al(OH)3↓?+2(NH4)2SO4
30、NaAlO2+HCl+H2O=Al(OH)3↓? +NaCl ; NaAlO2+CO2+H2O=Al(OH)3↓? +NaHCO3
31、高温下铁与水反应 :3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
32、FeCl3+3NaOH=Fe(OH)3↓?+3NaCl
33、4Fe(OH)2+O2+2H2O=4Fe(OH)3
34、2FeCl2+Cl2=2FeCl3 2FeCl3+Fe=3FeCl2
35、氯化铁溶液中加入铜粉: 2FeCl3+Cu=2FeCl2+CuCl2
36、金属的冶炼:Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
CuO+C![]() Cu+CO↑
Cu+CO↑
![]()
37、铜锌原电池:正极:2H++2e- =H2↑
负极:Zn-2e- =Zn2+
38、钢铁的吸氧腐蚀:正极:O2+4e- +2H2O=4OH-
负极:Fe-2e- =Fe2+
39、Fe(OH)3胶体的制取:FeCl3 +3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
40、电解CuCl2溶液:阳极:2Cl- -2e- =Cl2↑
阴极:Cu2++2e- =Cu
总反应:CuCl2![]() Cu+Cl2↑
Cu+Cl2↑
41、铜的电解精炼:阳极:Cu-2e- =Cu2+
阴极:Cu2++2e- =Cu
42、电镀铜:阳极:Cu-2e- =Cu2+
阴极:Cu2++2e- =Cu
43、电解饱和食盐水:阳极:2Cl- +2e-=Cl2↑
阴极:2H+ +2e- =H2↑
总反应:2NaOH+2H2O![]() H2↑+2NaOH+Cl2↑
H2↑+2NaOH+Cl2↑
44、黄铁矿的燃烧: 4FeS2 +11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
45、氨水吸收少量SO2: SO2+2NH3 +H2O=(NH4)2SO3
46、C+H2O(g)![]() CO+H2
CO+H2