摘要:荒漠化:指由气候和人类活动在内的种种因素造成的干旱.半干旱和亚湿润地区的土地退化.也就是由于大风吹蚀.流水浸蚀.土壤盐渍化等造成的土壤生产力下降或丧失.都称为荒漠化.土地荒漠化最终结果大多数是沙漠化.
网址:http://m.1010jiajiao.com/timu_id_189570[举报]
 (2011?江西)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:
(2011?江西)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:(1)用太阳能分解10mol水消耗的能量是
2858
2858
kJ;(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ?mol-1
CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ?mol-1
;(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);下列说法正确的是
③④
③④
(填序号)①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=
| nA |
| tA |
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时
| n(H2) |
| n(CH3OH) |
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为
| 2-a |
| 2 |
| 2-a |
| 2 |
(5)在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,负极的反应式为
CH3OH+H2O-6e-=CO2+6H+
CH3OH+H2O-6e-=CO2+6H+
,正极的反应式为| 3 |
| 2 |
| 3 |
| 2 |
96.6%
96.6%
(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比).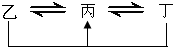 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:(1)写出化合物甲的电子式:


(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式
3NH3?H2O+Al3+=Al(OH)3↓+3NH4+
3NH3?H2O+Al3+=Al(OH)3↓+3NH4+
;写出均含有F元素的乙与丁在溶液中发生反应的离子方程式Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
.(3)由A、C元素组成的化合物戊和A、E元素组成的化合物己,式量均为34.其中戊的熔沸点高于己,其原因是:
H2O2分子间存在氢键
H2O2分子间存在氢键
.(4)复盐是指由2种或2种以上阳离子和一种酸根离子组成的盐.请写出由A、B、C、E、F元素组成的一种具有还原性的复盐庚的化学式
NH4)2Fe(SO4)2或(NH4)2Fe(SO4)2?6H2O或(NH4)2SO4?FeSO4?6H2O
NH4)2Fe(SO4)2或(NH4)2Fe(SO4)2?6H2O或(NH4)2SO4?FeSO4?6H2O
.该复盐是一种重要的化学试剂,据中学课本介绍,工业上常用如下方法制取:将一定量的两种盐配成混合溶液,再加热浓缩混合溶液,冷却至室温则析出带有6个结晶水的该复盐晶体.写出相关反应的化学方程式(NH4)2SO4+FeSO4+6H2O=(NH4)2Fe(SO4)2?6H2O
(NH4)2SO4+FeSO4+6H2O=(NH4)2Fe(SO4)2?6H2O
,析出该复盐晶体的原理是硫酸亚铁铵在水中溶解度比硫酸铵、硫酸亚铁在水中的溶解度要小得多
硫酸亚铁铵在水中溶解度比硫酸铵、硫酸亚铁在水中的溶解度要小得多
.2013年12月2日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥三号”探月卫星成功送入太空,进一步向广寒宫探索.“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂.
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂.但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体).
已知:N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-543kJ?mol-1;
H2(g)+
F2(g)═HF(g),△H=-269kJ?mol-1;H2(g)+
O2(g)═H2O(g),△H=-242kJ?mol-1
请写出肼和氟气反应的热化学方程式: .
Ⅱ.氧化剂二氧化氮可由NO和O2生成,已知在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2ΝΟ2(g)△H的体系中,n(NO)随时间的变化如表:
(1)已知:K800℃>K1000℃,则该反应的△H 0(填“大于”或“小于”),用O2表示从0~2s内该反应的平均速率为 .
(2)能说明该反应已达到平衡状态的是 .
a.容器内颜色保持不变 b. 2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有 .
(4)在上述条件下,计算通入2mol NO和1mol O2的平衡常数K= .
(5)在上述条件下,若开始通入的是0.2mol NO2气体,达到化学平衡时,则NO2的转化率为 .
查看习题详情和答案>>
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂.但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体).
已知:N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-543kJ?mol-1;
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
请写出肼和氟气反应的热化学方程式:
Ⅱ.氧化剂二氧化氮可由NO和O2生成,已知在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2ΝΟ2(g)△H的体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
| n(O2)(mol) | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(2)能说明该反应已达到平衡状态的是
a.容器内颜色保持不变 b. 2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有
(4)在上述条件下,计算通入2mol NO和1mol O2的平衡常数K=
(5)在上述条件下,若开始通入的是0.2mol NO2气体,达到化学平衡时,则NO2的转化率为
“生物质“是指由植物或动物生命体衍生得到的物质的总称.“生物质能”是人类解决能源危机的一种重要的能源.“生物质”在一定条件下可气化为CO、H2等原料气,进而合成甲醇和二甲醚(CH3OCH3),相关反应为:①2H2(g)+CO(g)?CH3OH(g) ②4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)
请根据图1所示回答问题:
(1)由H2和CO合成二甲醚的热化学方程式是 .
(2)在T1、T2温度下,向两个容积相同的密闭容器中分别通入1molCO和2molH2合成甲醇,则T1、T2温度下对应反应的平衡常数K1 K2 (选填“<”、“>”或“=”).
(3)在一定条件下,向一个容积可变的密闭容器中充入4molH2、2molCO、1molCH3OCH3(g)和1molH20(g),经一定时间反应②达到平衡状态,此时测得混合气体的密度是起始时的1.6倍.反应开始时正、逆反应速率的大小关系为V(正) V(逆)(选填“>”、“<”或“=”),平衡时n(CH3OCH3)= mol.
(4)如图2为绿色电源“二甲醚燃料电池”的工作原理示意图.(a、b均为多孔性Pt电极)b电极是 极.(填“正”或“负”)
a电极上的电极反应为 .
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6.现将c mol?L-1CaCl2溶液与2.00×10-2mol?L-1Na2S04溶液等体积混合(忽略体积的变化>,则生成沉淀时,c的最小值是 .
查看习题详情和答案>>
请根据图1所示回答问题:

(1)由H2和CO合成二甲醚的热化学方程式是
(2)在T1、T2温度下,向两个容积相同的密闭容器中分别通入1molCO和2molH2合成甲醇,则T1、T2温度下对应反应的平衡常数K1
(3)在一定条件下,向一个容积可变的密闭容器中充入4molH2、2molCO、1molCH3OCH3(g)和1molH20(g),经一定时间反应②达到平衡状态,此时测得混合气体的密度是起始时的1.6倍.反应开始时正、逆反应速率的大小关系为V(正)
(4)如图2为绿色电源“二甲醚燃料电池”的工作原理示意图.(a、b均为多孔性Pt电极)b电极是
a电极上的电极反应为
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6.现将c mol?L-1CaCl2溶液与2.00×10-2mol?L-1Na2S04溶液等体积混合(忽略体积的变化>,则生成沉淀时,c的最小值是