摘要:物质的制备:如Al2S3不能用湿法制备.
网址:http://m.1010jiajiao.com/timu_id_189502[举报]
氨、肼(N2H4)和叠氮酸都是氮元素的重要氢化物.

(1)氨可用于制造氮肥、硝酸等.
①合成氨工业中,“造气”有关反应的热化学方程式如下:
C(s)+H2O(g)=CO(g)+H2(g)△H1=+131.4kJ?mol-1
C(s)+2H2O(g)=CO2(g)+2H2(G)△H2=+90.2kJ?mol-1
CO(g)+H2O(g)=CO2(g)+H2(g)△H3
则△H3= .
②在一密闭容器中,加入物质的量之比为1:3的N2与H2,在不同温度、压强下测得平衡体系中NH3的物质的量分数如图1所示.则温度为400℃、压强为500×105 Pa时,H2的平衡转化率最接近 (填序号).
A.89% B.75%
C.49% D.34%
③实际生产中,合成氨的温度一般控制在400~500℃,选择该温度范围的理由是 .
④饮用水氯化消毒时若水中含有氨则会产生氯胺(NH2Cl、NHCl2等),氯胺水解缓慢释放出HClO,有良好的消毒效果.图2是饮用水氯化消毒时有关成分的含量与pH的关系.下列说法正确的是 (填序号).
A.HCIO在20℃的电离程度一定大于0℃的电离程度
B.pH越大,消毒效果越好
C.用NH2Cl消毒时,平衡NH2Cl+H2O?NH3+HClO向右移动
(2)肼可用于火箭燃料、制药原料等.
①次氯酸钠与过量的氨反应可以制备肼,该反应的化学方程式为 .
②一种肼燃料电池的工作原理如图3所示.该电池工作时负极的电极反应式为 .
③肼与亚硝酸(HNO2)反应可生成叠氮酸.8.6g叠氮酸完全分解可放出6.72L氮气(标准状况下),则叠氮酸的分子式为 .
查看习题详情和答案>>

(1)氨可用于制造氮肥、硝酸等.
①合成氨工业中,“造气”有关反应的热化学方程式如下:
C(s)+H2O(g)=CO(g)+H2(g)△H1=+131.4kJ?mol-1
C(s)+2H2O(g)=CO2(g)+2H2(G)△H2=+90.2kJ?mol-1
CO(g)+H2O(g)=CO2(g)+H2(g)△H3
则△H3=
②在一密闭容器中,加入物质的量之比为1:3的N2与H2,在不同温度、压强下测得平衡体系中NH3的物质的量分数如图1所示.则温度为400℃、压强为500×105 Pa时,H2的平衡转化率最接近
A.89% B.75%
C.49% D.34%
③实际生产中,合成氨的温度一般控制在400~500℃,选择该温度范围的理由是
④饮用水氯化消毒时若水中含有氨则会产生氯胺(NH2Cl、NHCl2等),氯胺水解缓慢释放出HClO,有良好的消毒效果.图2是饮用水氯化消毒时有关成分的含量与pH的关系.下列说法正确的是
A.HCIO在20℃的电离程度一定大于0℃的电离程度
B.pH越大,消毒效果越好
C.用NH2Cl消毒时,平衡NH2Cl+H2O?NH3+HClO向右移动
(2)肼可用于火箭燃料、制药原料等.
①次氯酸钠与过量的氨反应可以制备肼,该反应的化学方程式为
②一种肼燃料电池的工作原理如图3所示.该电池工作时负极的电极反应式为
③肼与亚硝酸(HNO2)反应可生成叠氮酸.8.6g叠氮酸完全分解可放出6.72L氮气(标准状况下),则叠氮酸的分子式为
 现有MgCl2和Al2(SO4)3的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量与加入NaOH的物质的量关系如图所示,则原溶液中Cl-与SO42-的物质的量之比为( )
现有MgCl2和Al2(SO4)3的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量与加入NaOH的物质的量关系如图所示,则原溶液中Cl-与SO42-的物质的量之比为( )
查看习题详情和答案>>
二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.

(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=
(2)汽车尾气中的主要污染物有CO、NOx、碳氢化合物等,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
生成无毒物质,减少汽车尾气污染.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图1所示,则
①前15s内的平均反应速率v (N2)=
②该反应平衡常数K=
③若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
a 加入催化剂 b 降低温度 c 缩小容器体积 d 增加CO2的量
④该可逆反应△S
(3)CO分析仪以燃料电池为工作原理,其装置如图2所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42- 而实现对SO2的处理目的.其中Fe3+的最外层电子排布式为
(5)N2O5是重要的硝化剂和氧化剂,可用电解法制备N2O5,如图3所示,N2O5在电解池的
查看习题详情和答案>>

(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=
-867 kJ/mol
-867 kJ/mol
;(2)汽车尾气中的主要污染物有CO、NOx、碳氢化合物等,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
生成无毒物质,减少汽车尾气污染.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图1所示,则
①前15s内的平均反应速率v (N2)=
0.013 mol/(L?s)
0.013 mol/(L?s)
(小数点保留3位);②该反应平衡常数K=
0.035
0.035
(小数点保留3位);③若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
不移动
不移动
移动(填“向左”、“向右”或“不”);20min时,若改变反应条件,导致N2浓度发生如图1所示的变化,则改变的条件可能是b
b
(填序号);a 加入催化剂 b 降低温度 c 缩小容器体积 d 增加CO2的量
④该可逆反应△S
<
<
0(填“>”、“<”或“=”),在低温
低温
(填“高温”、“低温”或“任何温度”)下能自发进行.(3)CO分析仪以燃料电池为工作原理,其装置如图2所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是
B
B
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42- 而实现对SO2的处理目的.其中Fe3+的最外层电子排布式为
3s23p63d5
3s23p63d5
;SO2的VSEPR模型名称为平面三角形
平面三角形
;与SO2互为等电子体的离子有NO2-
NO2-
.(5)N2O5是重要的硝化剂和氧化剂,可用电解法制备N2O5,如图3所示,N2O5在电解池的
阳极
阳极
(填“阳极”或“阴极”)区生成,其电极反应式为N2O4-2e-+2HNO3=2N2O5+2H+
N2O4-2e-+2HNO3=2N2O5+2H+
.
硫代硫酸钠(Na2S2O3,在酸性溶液中不能稳定存在)可由亚硫酸钠和硫粉通过化合反应制得,装置如图Ⅰ;有关物质的溶解度曲线如图Ⅱ所示.
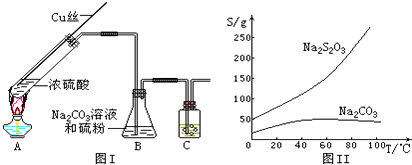
(1)Na2S2O3?5H2O的制备:
①写出试管内发生反应的化学方程式: .
②B中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当B中溶液的pH接近7时就停止加热,理由是 ;装置C的作用是 .
③过滤B中的混合液,将滤液经过 、 、过滤、洗涤、烘干,得到产品.
(2)饱和Na2CO3溶液吸收少量SO2后所得溶液呈弱碱性,含有OH-、SO32-、HCO3-等阴离子.
请设计试验方案,证明“滤液”中存在SO32-、HCO3-,在答题卡上写出实验步骤、预期现象和结论.
限选仪器及试剂:pH计、小烧杯、试管、带塞导气管、滴管、玻璃棒、过滤装置和滤纸;2mol/L盐酸、1mol/LBaCl2溶液、1 mol/LBa(NO3)2溶液、品红溶液、紫色石蕊试液、澄清石灰水等.
查看习题详情和答案>>

(1)Na2S2O3?5H2O的制备:
①写出试管内发生反应的化学方程式:
②B中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当B中溶液的pH接近7时就停止加热,理由是
③过滤B中的混合液,将滤液经过
(2)饱和Na2CO3溶液吸收少量SO2后所得溶液呈弱碱性,含有OH-、SO32-、HCO3-等阴离子.
请设计试验方案,证明“滤液”中存在SO32-、HCO3-,在答题卡上写出实验步骤、预期现象和结论.
限选仪器及试剂:pH计、小烧杯、试管、带塞导气管、滴管、玻璃棒、过滤装置和滤纸;2mol/L盐酸、1mol/LBaCl2溶液、1 mol/LBa(NO3)2溶液、品红溶液、紫色石蕊试液、澄清石灰水等.
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“滤液”于小烧杯中,用滴管向小烧杯加入过量l mol/L BaCl2溶液. | 若出现白色浑浊,溶液可能存在SO32-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,将所得固体、滤液分别置于试管A、B备用. | / |
| 步骤3:向试管A中加入 |
|
| 步骤4:向试管B中加入 |
已知:H2A的A2-可表示S2-、S
、S
、Si
或C
离子.
(1)常温下,向20mL 0.2mol?L-1 H2A溶液中滴加0.2mol?L-1 NaOH溶液.有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).请根据图示填空:
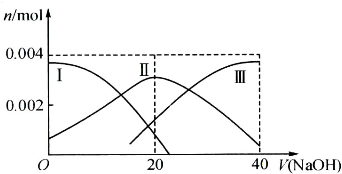
①当V(NaOH)=20mL时,溶液中离子浓度大小关系: ;
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水 (填“大”、“小”或“相等”),欲使NaHA溶液呈中性,可以向其中加入 .
(2)有关H2A的钠盐的热化学方程式如下:
①Na2SO4(s)═Na2S(s)+2O2(g)△H1=+1011.0kJ?mol-1;
②2C(s)+O2(g)═2CO(g)△H2=-221.0kJ?mol-1.
则Na2SO4(s)+4C(s)═Na2S(s)+4CO(g)△H3= kJ?mol-1;
工业上制备Na2S时往往要加入过量的碳,同时还要通入空气,目的有两个,其一是利用碳与氧气反应放出的热维持反应所需温度,其二是 .
(3)若H2A为硫酸:t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW= .
查看习题详情和答案>>
| O | 2- 4 |
| O | 2- 3 |
| O | 2- 3 |
| O | 2- 3 |
(1)常温下,向20mL 0.2mol?L-1 H2A溶液中滴加0.2mol?L-1 NaOH溶液.有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).请根据图示填空:

①当V(NaOH)=20mL时,溶液中离子浓度大小关系:
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水
(2)有关H2A的钠盐的热化学方程式如下:
①Na2SO4(s)═Na2S(s)+2O2(g)△H1=+1011.0kJ?mol-1;
②2C(s)+O2(g)═2CO(g)△H2=-221.0kJ?mol-1.
则Na2SO4(s)+4C(s)═Na2S(s)+4CO(g)△H3=
工业上制备Na2S时往往要加入过量的碳,同时还要通入空气,目的有两个,其一是利用碳与氧气反应放出的热维持反应所需温度,其二是
(3)若H2A为硫酸:t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW=