摘要:(2)强碱混合: 然后.再根据c(H+)= Kw/ c(OH-).求算c(H+).
网址:http://m.1010jiajiao.com/timu_id_189482[举报]
(1)已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得溶液呈酸性:0.01mol?L-1的HIO3或HMnO4溶液与pH=12的Ba(OH)2溶液等体积混合所得溶液均呈中性.
①H5IO6是 电解质(填“强”或“弱”)
②已知H5IO6和MnSO4在溶液中反应生成高锰酸、碘酸和硫酸,反应的离子方程式为
(2)25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白:
①a值不可能等于3,其理由是
②a值可否等于5 (填“可”或“否”),其理由是
③a的取值范围是 .
查看习题详情和答案>>
①H5IO6是
②已知H5IO6和MnSO4在溶液中反应生成高锰酸、碘酸和硫酸,反应的离子方程式为
(2)25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白:
①a值不可能等于3,其理由是
②a值可否等于5
③a的取值范围是
CuSO4溶液与Na2CO3溶液混合产生蓝绿色沉淀,以下是某兴趣小组对沉淀组成的探究.
提出假设:
假设1:沉淀为Cu (OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3?mCu (OH)2]
查阅资料:
无论是哪一种沉淀受热均易分解(假设均不含结晶水).
定性探究:
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如下装置(夹持仪器未画出)进行定性实验;
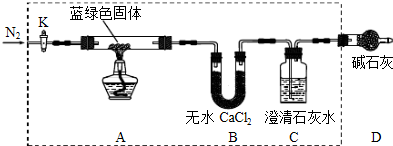
(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设 成立.
(2)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是 (填代号).
a.浓硫酸 b.无水CuSO4 c.碱石灰 d.P2O5
(3)乙同学更换B试剂后验证假设3成立的实验现象是 .
定量探究
(4)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在20℃的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是 (双选,填代号)
a.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
b.Ba(OH)2为强碱,Ca(OH)2为弱碱
c.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
d.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为54.2g,实验结束后装置B的质量增加5.4g,C中的产生沉淀的质量为39.4g.则该蓝绿色固体的化学式为 .
查看习题详情和答案>>
提出假设:
假设1:沉淀为Cu (OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3?mCu (OH)2]
查阅资料:
无论是哪一种沉淀受热均易分解(假设均不含结晶水).
定性探究:
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如下装置(夹持仪器未画出)进行定性实验;

(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设
(2)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是
a.浓硫酸 b.无水CuSO4 c.碱石灰 d.P2O5
(3)乙同学更换B试剂后验证假设3成立的实验现象是
定量探究
(4)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在20℃的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是
| 溶解度(S)/g | 溶度积(Ksp) | 摩尔质量(M)/g?mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
b.Ba(OH)2为强碱,Ca(OH)2为弱碱
c.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
d.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为54.2g,实验结束后装置B的质量增加5.4g,C中的产生沉淀的质量为39.4g.则该蓝绿色固体的化学式为
常温下,将某一元碱BOH和HCl溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从第①组情况分析,BOH是
(2)第②组情况表明,c
(3)从第③组实验结果分析,混合溶液中 (选填“<”、“>”或“=”)
甲:BOH的电离程度
查看习题详情和答案>>
| 实验编号 | HCl的物质的量浓度 (mol?L-1) |
BOH的物质的量浓度 (mol?L-1) |
混合溶液的pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH>7 |
(1)从第①组情况分析,BOH是
弱碱
弱碱
(选填“强碱”或“弱碱”).该组所得混合溶液中由水电离出的c(OH-)=10-5
10-5
mol?L-1.(2)第②组情况表明,c
<
<
0.2.该混合液中离子浓度c(B+)=
=
c(Cl-)(选填“<”、“>”或“=”).(3)从第③组实验结果分析,混合溶液中 (选填“<”、“>”或“=”)
甲:BOH的电离程度
>
>
BCl的水解程度;乙:c(B+)-2c (OH-)=
=
c(BOH)-2c(H+)